Г.А. Самсыгина, Г.С. Коваль
ГОУ ВПО Российский государственный медицинский университет Росздрава, Москва
Инфекции дыхательных путей представляют серьезную проблему, особенно в детском возрасте. Так, в 2005-2006 гг. по данным Федерального центра Госсанэпиднадзора РФ заболеваемость острыми респираторными инфекциями среди детей составила чуть меньше 50 000 случаев на 100 000 детского населения, что более 70% регистрируемой инфекционной патологии детского возраста [1]. Причем, наиболее высокая заболеваемость отмечается в возрасте первых 6-7 лет жизни и причин тому несколько.
Во-первых, у детей раннего возраста, биоценоз верхних дыхательных путей находится в процессе становления, причем микробный пейзаж весьма нестабилен, полиморфен, зависим от окружающей среды и приближается к таковому взрослого человека только к 5–8 годам жизни [2]. Во-вторых, иммунная система детей раннего возраста, характеризуется высокой пролиферативной активностью лимфоцитов, причем фракция недифференцированных, «наивных» лимфоцитов у детей этого возраста больше, чем у взрослых. В-третьих, известно, что именно в возрасте 1,5-3 лет происходит переориентация иммунного ответа на инфекционные агенты с превалирования Th2 пути ответа, свойственного плодам, новорожденным и детям первых месяцев жизни, на Th1 ответ, типичный для инфекционного процесса у взрослого человека, т.е. происходит функциональное созревание противоинфекционного иммунитета ребенка. В-четвертых, важной особенностью иммунной системы детей раннего и дошкольного возрастов является состояние лимфоэпителиальной ткани глоточного кольца, осуществляющего местную противоинфекционную защиту респираторного тракта.
Известно, что именно в раннем детстве формируется лимфоэпителиальная глоточная система (ЛЭГС). Начиная со второго полугодия первого года жизни, постепенно формируются небные миндалины. На втором году начинается формирование глоточной миндалины (аденоиды), которая локализуется в так называемой «стратегической зоне» верхних дыхательных путей, там, где регистрируется наиболее интенсивное антигенное воздействие [2, 3]. ЛЭГС обладает выраженной лимфопоэтической функцией, участвует в производстве и «обучении» В-лимфоцитов для «своего региона» – слизистой оболочки дыхательных путей, – где они осуществляют местную продукцию IgA и IgM. Эпителиоциты слизистой оболочки носоглотки и миндалин образуют петлистую сеть, где сосредотачиваются мигрирующие из общего кровотока лимфоциты. Проходя между эпителиальными клетками, лимфоциты нарушают целостность эпителиального покрова, образуя так называемые «ходы», которые обеспечивают контакт лимфоидной ткани глотки и миндалин с внешней средой. Именно эти внутриэпителиальные ходы «дозируют» поступление антигенов в ЛЭГС, обеспечивая адекватную антигенную нагрузку на лимфоидный аппарат глотки [2, 3]. При нарушении целостности эпителия под воздействием инфекции, особенно повторной, антигенная нагрузка на ЛЭГС неизмеримо возрастает. Это может сопровождаться перенапряжением, истощением или расстройством защитных механизмов.
Функциональная активность ЛЭГС зависит от возраста: у здоровых детей максимум увеличения небных миндалин приходится на возраст 3–5 лет, а увеличение глоточной миндалины (аденоидов) – на возраст 5–7 лет. После этих «пиков» отмечается постепенная редукция ЛЭГС, завершающаяся обычно к 18 годам [3].
Эти особенности иммунной системы организма ребенка раннего и дошкольного возрастов являются факторами, обуславливающими их более высокую, чем в старшем возрасте и во взрослом состоянии, заболеваемость респираторными, особенно вирусными, инфекциями.
При респираторных инфекциях, повторяющихся более 6-8 раз в год, адекватного восстановления функциональных характеристик иммунной системы, по-видимому, не происходит. Этим характеризуется так называемая группа часто болеющих детей (ЧБД). Исследования иммунного статуса у большинства ЧБД выявили неспецифичные изменения противоинфекционной защиты [4-8]. Даже в период клинического благополучия и при отсутствии острой респираторной инфекции (ОРИ) у них оказалось достоверно повышенным содержание провоспалительных интерлейкинов (IL2, IL4), в том числе интерлейкинов, участвующих в хронизации процессов воспаления (IL6, IL8) и снижено содержание интерферона (ИФН), особенно ИФН?. При этом индуцированная продукция провоспалительных цитокинов недостаточна, что свидетельствует об истощении резервных возможностей иммунной системы организма ребенка. Снижение количества CD11b клеток, куда входят гранулоциты, моноциты, натуральные киллеры и макрофаги, экспрессирующие молекулы межклеточной адгезии, а также уменьшение количества эндотелиальных клеток, экспрессирующих межклеточные молекулы адгезии 1 типа и рецепторы к риновирусам во многом объясняет повышение чувствительности детей к повторным респираторным вирусным инфекциям [5, 6].
По данным различных авторов и данным всеобщей диспансеризации 2002 г. [9, 12] ЧБД составляют в общей популяции детского населения в среднем 5% , хотя некоторые авторы приводят более высокие показатели – до 65% [10-15]. Наиболее высокая частота выявления ЧБД отмечается в возрасте 2-3-х лет – 10-15%, наименьшая – в 17 лет, – 3% детей [9, 12]. Хотя в своем последнем обзоре А.Л. Заплатников и Н.А. Коровина отмечают, что, ориентируясь только на официально зарегистрированные эпизоды ОРИ, нельзя судить об истинной частоте респираторных инфекций у ребенка [16]. Возможна как гиподиагностика ЧБД, так и гипердиагностика.
Некоторые авторы считают, что всех ЧБД следует делить на три группы [17]. I группу составляют дети, у которых ОРИ, как правило, протекают в легкой форме и выздоровление обычно происходит в короткие сроки. Осложнения возможны, но редки. Чаще всего дети начинают болеть в конце первого или на втором году жизни. Т.В. Праздникова [18], наблюдая в катамнезе детей различного гестационного возраста, перенесших в неонатальном периоде синдром дыхательной дисфункции, по поводу которого им проводилась искусственная вентиляция легкий, отмечает, что 24,7% этих детей были ЧБД, причем именно в возрасте до 3 лет, в основном в виде ОРИ с быстрым выздоровлением и без осложнений. Характерно, что в основном это были глубоко недоношенные дети. Только 9,5% ЧБД были доношенными.
У большинства детей (у 70%) в возрасте после трех лет при благоприятной обстановке частота ОРИ снижается. В неблагоприятных условиях повторные ОРИ сохраняются до 5-6 летнего возраста, редко дольше. Физическое и психомоторное развитие детей соответствует возрастной норме.
Это основная часть ЧБД, она составляет около 40% детей часто болеющих ОРИ.
II группа, приблизительно 20-25% ЧБД, характеризуется тем, что ОРИ у них протекают с длительным выздоровлением. После выздоровления у детей отмечается недомогание, снижение аппетита, нарушение ритма сон-бодрствование, бледность и др. На фоне этих изменений вновь возникают ОРИ, которые превращают заболевание в волнообразный процесс без полной нормализации состояния. Иногда процесс сразу приобретает тяжелое течение с наличием осложнений. Дети болеют независимо от посещения дошкольных учреждений. Как правило, частота ОРИ уменьшается в возрасте после 5-7 лет. В 1,5-2 года у большинства детей выявляется гипертрофия миндалин и аденоидов [10, 12, 13, 15]. В анамнезе удается выявить у одного или обоих родителей ребенка склонность к частым респираторным заболеваниям. Предполагается, что причиной такого состояния являются генетически обусловленная задержка созревания иммунной системы и неблагоприятные факторы окружающей среды. Но нельзя исключать и первичные парциальные иммунодефициты, о которых в последние годы пишется в основном в зарубежной литературе [31]. Из-за наследственной предрасположенности заболеваемость у этих детей является трудно управляемой [14].
III группа ЧБД отличается наличием ЛОР – патологии, как ведущего фактора развития респираторных заболеваний. Они составляют 30-35% случаев. Время начала повторных ОРИ – возраст после 1 года. Дети болеют независимо от посещения дошкольных учреждений. С 2-3 лет в течение ОРИ отмечают чередование обострений и неполных ремиссий, во время которых сохраняется затрудненное носовое дыхание и ночной кашель. При осмотре у ЛОР врача чаще всего выявляются аденоидит, тонзиллит, отит и др. При отсутствии лечения у многих развиваются трахеиты, бронхиты, пневмонии. Снижение частоты ОРИ зависит от адекватности лечения соответствующих очагов инфекции (аденоидит, тонзиллит и др.). У родственников также прослеживается патология ЛОР – органов. Физическое развитие детей, как правило, не нарушено [10, 15, 19].
Таким образом, у 40% ЧБД эти частые, практически ежемесячные, ОРИ не представляют ничего иного как последовательные вирусные инфекции, что, по-видимому, в значительной степени обусловлено возрастным созреванием иммунной системы ребенка и перенапряжением и относительным истощением иммунной функции ЛЭГС. Для этих детей, с неосложненной частой заболеваемостью ОРИ, показано, прежде всего, проведение общегигиенических мероприятий [19]. Это:
Организация рационального режима дня ребенка:
- полноценный, достаточный по длительности сон,
- исключение переутомления и перевозбуждения,
- обязательные и достаточные по длительности прогулки, но без переохлаждения,
- ограничение посещения мест большего скопления людей и т.д.
- Исключение пассивного табакокурения ребенка в семье.
- Полноценное питание, учитывающее возрастные особенности ребенка, склонность его к аллергическим реакциям. Использование пищи богатой цинком, железом, т.к. нет сомнений в отношении того, что недостаток цинка и железа увеличивают предрасположенность ребенка к респираторным инфекциям [20, 21].
- Прием поливитаминных препаратов, соответствующих возрасту ребенка и его нагрузкам, профилактика и лечение дефицита железа [20] и дефицита цинка [21, 22].
- Наконец, проведение в разумных пределах закаливающих мероприятий, таких как обливания прохладной водой, сон на свежем воздухе, ванны, души, бальнеотерапия, общий массаж, лечебная гимнастика, тренирующие занятия физкультурой.
Luby S.P.
и соавт. в ряду общегигиенических мероприятий обращают большое внимание на мытьё рук детей с мылом [23, 24], доказывая в рандомизиронном контролируемом исследовании, что мытьё рук с мылом предотвращает эпидемиологически обусловленную заболеваемость респираторными инфекциями у ЧБД (рис.1). Надо сказать, что несколько ранее MeadowsE. и LeSauxN. опубликовали мета-анализ 6 исследований, 2 из которых были рандомизированными контролируемыми исследованиями, по использованию бактерицидных гелей для рук, содержащих антибиотики, которые использовались у младших ЧБ школьников [25]. Это, по мнению авторов, также способствовало снижению частоты ОРИ у ЧБД в эпидемиологический сезон года.
Совсем иная картина частых ОРИ развивается у детей, страдающих аллергией, которая, как известно, характеризуется поляризацией иммунного ответа в сторону Th2 ответа. Следовательно, физиологические Th1-зависимые механизмы борьбы с респираторными инфекциями могут быть нарушены. Дети с аллергическими заболеваниями (атопический дерматит, респираторная аллергия) могут часто болеть ОРИ в грудном возрасте и раннем детстве и, следовательно, могут быть отнесены в группу ЧБД. Ciprandi G. [26] исследовал частоту и длительность респираторных инфекций у детей с аллергическими заболеваниями и без таковых. Было показано, что у детей, страдающих аллергическими заболеваниями, значимо увеличивались количество, длительность и тяжесть респираторных инфекций в сравнении с детьми без аллергии.
Однако это не исключает, что довольно часто участковыми педиатрами обострения аллергических заболеваний дыхательных путей расцениваются как простые ОРИ и ребенок многократно получает необоснованную терапию [16, 27-29]. Это, вероятно, связано с тем, что имеются определенные трудности в трактовке респираторных инфекций у детей, страдающих аллергией. Известно, что при аллергии респираторной системы у ребенка вирусы являются наиболее частой причиной обострения основного (аллергического) заболевания и проведение дифференциальной диагностики ОРИ и аллергического ринита, фарингита, ларингита, трахеита у детей раннего возраста, страдающих аллергией, становится насущной необходимостью. Например, при обострении аллергического ринита, связанного с вирусной инфекцией, может наблюдаться нарушение самочувствия, выделения из носа в виде «молочной пены», отек кончика носа, мацерация кожи вокруг носа, даже лихорадка, что служит основанием для ошибочной диагностики простого ОРИ у ЧБ ребенка.
Для того чтобы избежать подобных диагностических ошибок, первое, что врачу-педиатру необходимо сделать, это собрать или уточнить семейный анамнез и аллергологический анамнез самого больного: связь рецидивов ОРИ с причинно-значимыми аллергическими факторами, оценить рецидивирующий бронхообструктивный синдром, правильно оценить низкий эффект или его полное отсутствие при проведении только противовирусной и антибактериальной терапии. Во-вторых, при подозрении на аллергическую природу респираторных проявлений больному ОРИ после выздоровления показано аллергологическое обследование. Алллергологическое обследование предполагает у ребенка в возрасте до трех лет обследование на общий IgE и специфичные IgE; в возрасте после трех лет кожные тесты (prick тест) или специфичные тесты Phadiatop.
Phadiatop (Pharmacia differentiate atopy) – объективный тест для проведения анализа на наличие у пациента аллергии, чувствительность теста составляет 93%, а специфичность – 89%. Тест представляет собой сбалансированную смесь наиболее распространенных ингаляционных аллергенов [30].
Кроме того, необходимо направить ребенка на консультацию аллерголога, т.к. ранняя диагностика аллергических заболеваний дыхательных путей очень важна для назначения адекватной противоаллергической терапии.
Очевидно, что дети, страдающие аллергией, в основном входят во 2 группу ЧБД, т.к. именно у этих детей, особенно когда аллергия респираторного тракта не установлена и ребенок не получает специфической антиаллергической терапии, частые респираторные инфекции протекают более тяжело, период ремиссии непродолжителен и протекает с изменением состояния пациентов, а ОРИ часто сопровождаются бактериальными осложнениями. Кроме того, как показали в основном зарубежные исследования в последние годы, в эту же 2 группу, а также в 3 группу ЧБД в сочетании с хронической ЛОР – патологией, входят дети с нераспознанными парциальными первичными иммунодефицитами [31].
Сочетание ОРИ с ЛОР – патологией отмечается, как уже говорилось, у 30-35% ЧБД. Здесь на первое место выступает именно ЛОР – патология: хронический аденоидит, хронический и рецидивирующий тонзиллит, рецидивирующие отиты, рецидивирующие синуситы, а также именно у этих детей отмечаются рецидивирующие бронхиты и даже рецидивирующие пневмонии. Наиболее распространенное международное определение рецидивирующего тонзиллита (ангин) – это семь или более эпизодов в течение одного года или десять в течение двух-трех последних лет;
рецидивирующий отит: три эпизода в течение шести месяцев или четыре эпизода за год; рецидивирующий синусит: 2 эпизода за год [31].
В отношении пневмонии два эпизода за год рассматриваются как рецидивирующие пневмонии при условии, что рентгенография грудной клетки была без патологии между эпизодами. Что касается ларингитов и бронхитов, то международно принятых определений не существует [31].
Дети с сочетанием ЛОР – патологии и частых респираторных инфекций нуждаются в наблюдении отоларинголога и дополнительном уточнении анамнеза жизни и заболевания ребенка и обследовании, которое проводится также отоларингологом. Это – назофаринегеальная фиброскопия при явном аденоидите. Ее цель заключается в уточнении состояния аденоидных вегетаций и выявлении опосредованных признаков гастро-эзофагального рефлюкса, если таковой имеется. При синуситах отоларингологическое обследование включает рентгенографию придаточных пазух носа, а также грудной клетки и тест на пот для исключения муковисцедоза. Затем может быть проведено сканирование пазух на выявление костных пороков носовых пазух или минимального полипоза. И наконец, при отрицательном предшествующем обследовании и непреходящем характере синусита у ребенка показано проведение биопсии слизистой носовой полости в целях исключения цилиарной примитивной дискинезии [31, 32].
Уточнение анамнеза жизни и заболевания ребенка, проведение дополнительных методов обследования позволяют вычленить из группы ЧБД такие заболевания, как гастро-эзофагальный рефлюкс, бронхолегочная дисплазия, вторичный хронический бронхит, муковисцидоз, бронхоэктатическая болезнь, врожденные пороки развития легких, первичная цилиарная дискинезия, которые нередко рассматриваются как частые ОРИ у ЧБД.
Если у ЧБ ребенка хроническая ЛОР – патология подтверждена то там имеется очаг хронической инфекции и, следовательно, наряду с общими оздоровительными мероприятиями показано проведение местного отоларингологического лечения, объем которого определяется врачом – отоларингологом и зависит от характера, степени выраженности и топики поражения. Местная терапия направлена на санацию хронических очагов инфекции, восстановление целостности слизистых носоглотки, подавление хронического воспаления [19, 32]. Местная терапия включает:
- Орошения слизистых солевыми растворами типа Акве марис, физиомера, салина и др.
- Использование бактерицидных пастилок типа Стрепсилс, Бронхикум, Фарингосепт и др.
- Полоскание зава (у детей старше 4-5 лет) антисептическими растворами (гексорал, раствор фурацилина, отвары ромашки, зверобоя и т.д.), промывание носовых ходов, использование спрея гексорала.
- Физиотерапевтические методы (УФО на миндалины, УВЧ, СВЧ и гелий-неоновое лазерное облучение на регионарные лимфоузлы, ингаляции с морской водой, маслом эвкалипта и т.д.).
Если проведение этих процедур не улучшает состояния пациента, не дает положительного эффекта, то необходимо проведение обследования для выявления парциальных первичных иммунодефицитов. Сейчас известно свыше 150 первичных парциальных иммунодефицитов, часть из которых клинически напоминает простые ОРИ или ОРИ в сочетании с ЛОР – патологией. Так, дефицит подкласса IgG2 и/или изотипов Ig проявляется развитием у детей на фоне частых ОРИ рецидивирующих пневмоний и рецидивирующих синуситов; дефицит IgA приводит к развитию на фоне частых ОРИ пневмоний, рецидивирующих отитов, диареи; маннозо-связывающий лектин 2 (MBL2) активирует систему комплемента и способствует развитию на фоне частых ОРИ рецидивирующих отитов [33-36]. У детей с частыми ОРИ и рецидивирующими отитами описаны более низкие уровни антител к определенным серотипам пневмококка, чем у здоровых детей того же возраста [37]. Такие же результаты были описаны в отношении протеина Р6 [38] и т.д.
Bossuyt X. и соавт. [33] приводят данные, что при сочетании рецидивирующих инфекций респираторного тракта с ЛОР – патологией только у 10,9% детей не было выявлено какого-либо дефекта иммунитета, у 30,3% детей выявлен 1 дефект иммунитета, у 38,1% – два, а у 14,7% выявлено 3 дефекта иммунитета, что может быть, по мнению авторов, проявлением как иммунологической незрелости, так и первичными парциальными иммунодефицитами. Незрелость иммунной системы ребенка может проявляться временным иммунодефицитом. Он может быть в виде количественного и/или функционального дефицита Т-лимфоцитов, который проявляется изменениями в субпопуляциях Т-лимфоцитов, недостаточностью ответа на митогены, нарушением розеткообразования. Может быть временный дефицит иммуноглобулинов классов А и G; может быть дефицит хемотаксиса нейтрофилов, что считается результатом снижения выработки лимфокинов; может быть дефицит антимикробной активности. Особенностью незрелости иммунной системы ребенка является обратимость, временность выявленных изменений иммунной системы, в отличие от парциальных первичных иммунодефицитов, которые сопровождают пациента в течение всей последующей жизни.
Поэтому на следующем этапе обследования ЧБД из 2 и 3 группы надо определить содержание иммуноглобулинов (IgG и IgA), оценить реакции на вакцинальные антигены (столбняка, дифтерии, Hib), у детей старше двух лет определить содержание подклассов IgG (IgG2) и проконсультировать ребенка у иммунолога. Это позволит своевременно вычленить из группы ЧБД детей с парциальными иммунодефицитами и иммунологической незрелостью, клинически проявляющиеся рецидивирующими инфекциями верхних и нижних респираторных путей и нередко осложняющимися рецидивирующими отитами, рецидивирующими риносинуситами, рецидивирующими бронхитами и даже рецидивирующими пневмониями.
В лечении ЧБД 1-ой группы, которая характеризуется лишь частыми ОРИ, протекающими, как правило, без осложнений, но которые могут в силу частого повторения привести к истощению иммунной системы ребенка, большое значение имеет отечественный препарат Виферон, представляющий рекомбинантный препарат ?2В-интерферона в комплексе с антиоксидантами. Введенные в Виферон токоферол ацетат и аскорбиновая кислота, усиливают его противовирусную активность в 10-14 раз, что выгодно у ЧБД, а кроме того, усиливают действие рекомбинантного ?2В-интерферона на Т- и В-лимфоциты и нормализуют содержание IgE у ребенка [39]. Лекарственные формы Виферона в виде ректальных суппозиториев (свечей), геля и мази обеспечивают простые, безопасные и безболезненные способы его введения. Виферон можно назначать всем больным детям, включая новорожденных и недоношенных детей, в том числе и пациентам с аллергией [39].
Этот метод лечения (использование Виферона) по современной классификации иммуностимулирующей терапии (ИСТ) представляет неспецифическую активно-пассивную ИСТ, основная цель которой активация иммунной системы и усиление «общего» иммунитета больного [40]. Кроме того, в настоящее время имеются убедительные данные о высоком терапевтическом эффекте при лечении детей с ОРИ индукторами эндогенного интерферона (Арбидол, Циклоферон, Амиксин). Индукторы интерферона представляют собой разнородное по составу семейство высоко- и низкомолекулярных синтетических и природных соединений, объединенных способностью вызывать в организме образование собственного (эндогенного) интерферона. Но ограничением для их использования является то, что индукторы интерферона имеют возрастные ограничения. Арбидол может быть использован у детей начиная с 2,5-летнего возраста, Циклоферон разрешен для применения у детей старше 4 лет, а Амиксин — только у детей старше 7 лет.
К неспецифической активной ИСТ относят и нецитокиновые адъюванты – иммуномодуляторы микробного происхождения Имудон, Рибомунил, ИРС-19, Бронхомунал и др., которые можно использовать у ЧБД 1 группы, но более целесообразно их использование во 2 и 3 группах ЧБД. Все они обладают способностью усиливать функциональную активность нейтрофилов и макрофагов, а также обладают вакцинальным эффектом, который не только повышает активность неспецифических факторов иммунной защиты, но способствует формированию специфического иммунного ответа к наиболее значимым для респираторной патологии пневмотропным бактериальным возбудителям. К I поколению иммуномодуляторов микробного происхождения относятся лизаты полипатогенных микроорганизмов. Это – Бронхомунал, Имудон, ИРС-19. Их надо с осторожностью использовать у детей с аллергией. Ко II поколению иммуномодуляторов бактериального происхождения относятся частично очищенные компоненты лизатов полипатогенных микроорганизмов. Это – Рибомунил [40].
Проведенные в нашей стране исследования показали, что у ЧБД, получавших дополнительно к симптоматической терапии ОРИ, иммуномодулятор бактериального происхождения ИРС-19, по окончании курса лечения отмечается повышение ИФН? и снижение ИЛ4 и ИЛ8. Тогда как в группе контроля, не получавшей ИРС-19, содержание ИЛ8 и ИЛ4 не меняется или даже продолжает расти, а ИФН? – снижаться. Дети, получавшие терапию ИРС-19, стали в два раза реже болеть ОРИ, а длительность заболевания снизилась также в два раза [7, 8, 41].
Рибомунил, II поколение иммуностимуляторов бактериального происхождения, в состав которого входят не лизаты бактерий, а их рибосомы и фрагменты клеточной стенки, что повышает его эффективность и безопасность. Применение этого препарата характеризуется хорошей переносимостью, что позволяет значительно расширить возможности иммунокоррекции при оздоровлении ЧБД [14, 16].
В настоящее время у нас в стране появился новый иммуномодулятор, который представляет высокоочищенную синтетическую субстанцию дипептидной природы – пидотимод, действующее вещество препарата Имунорикс (фирма Солвей Фарма). Пидотимод характеризуется отсутствием токсических эффектов, быстрым всасыванием в желудочно-кишечном тракте, биодоступность его составляет 45%.
При воздействии на иммунитет ребенка точкой приложения пидотимода являются макрофаги, дендритные клетки, В-лимфоциты на стадии презентации антигена совместно с антигенами главного комплекса гистосовместимости 2 класса Т-лимфоцитов. Этот этап является важнейшим для реализации полного, завершенного иммунного ответа организма [42]. Пидотимод уменьшает экспрессию CD30, ассоциированного с Тh-2 лимфоцитами, и тем самым уменьшает аллергическую направленность иммунного ответа [43].
Пидотимод усиливает фагоцитарную активность полиморфноядерных лейкоцитов человека in vitro, а известна этиологическая роль дефицита фагоцитоза в полиморфноядерных нейтрофилах в развитии ОРИ у детей. Кроме того, пидотимод оказывает активирующее воздействие на различные типы иммунитета (врожденный и адаптивный иммунный ответ) [44-46].
Иммуномодулирующее действие препарата было подтверждено более чем в 60 международных контролируемых клинических исследованиях [47]. В настоящее время пидотимод (Имунорикс) рассматривается в качестве иммуномодулятора для 2 и 3 группы ЧБД, особенно для детей с незрелостью иммунитета.
Заключение.
Таким образом, несмотря на то, что группа ЧБД описана еще в 1986 году В.Ю. Альбицким и А.А. Барановым, до настоящего времени она представляет большую проблему в педиатрии, как в плане правильной диагностики, так и в плане адекватной терапии. Задача состоит в правильном и своевременном выявлении в амбулаторно-поликлиническом звене здравоохранения часто болеющих детей в сочетании с сопутствующими заболеваниями и без таковых. Незаменимую пользу в решении этой задачи приносят опрос, полное клиническое обследование ребенка и дополнительное клинико-лабораторное и инструментальное обследование, а также своевременные консультации других врачей – специалистов. Что касается использования иммуностимулирующей терапии у ЧБД, то её применение надо проводить дифференцировано в зависимости от группы ЧБД и тяжести острого респираторного заболевания с использованием различных иммуномодулирующих препаратов.
Литература.
Заплатников А.Л. Клинико-патогенетическое обоснование иммунотерапии и иммунопрофилактики вирусных и бактериальных заболеваний у детей. Автореф. дисс… докт. мед. наук. М., 2003.
http://immunologica.ru/?p=128
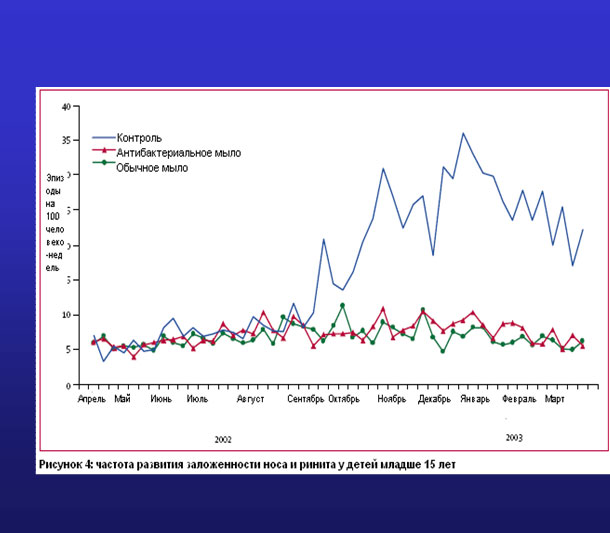 Рис. 1. Частота развития ОРИ у ЧБД младше 15 лет в зависимости от мытья рук [Luby S.P. et al. 2005].
Рис. 1. Частота развития ОРИ у ЧБД младше 15 лет в зависимости от мытья рук [Luby S.P. et al. 2005].



