У ребенка высокая температура, насморк, слабость… Знакомая картина? Многие родители в такой ситуации надеются на «волшебную таблетку» – антибиотик. А если инфекция вызвана вирусом? Тогда препарат не просто не поможет, но даже может навредить: уничтожит полезную микрофлору и приблизит момент, когда антибиотики перестанут работать вообще.
Согласно данным ВОЗ об устойчивости к антибиотикам, антибиотикорезистентность сегодня признана одной из главных угроз человечеству. К 2050 году устойчивые к антибиотикам инфекции могут уносить до 10 миллионов жизней ежегодно. И каждый необоснованный прием антибиотика вносит свой вклад в эту статистику.
Почему не нужно принимать антибиотики при гриппе? Возможно ли лечение ОРВИ без антибиотиков? Какие противовирусные средства существуют? И почему препараты с неспецифическим действием – в первую очередь интерфероны – становятся важным инструментом разумной защиты? Ответы на эти вопросы помогают сформировать четкий алгоритм действий: когда нужен антибиотик, когда – противовирусные лекарства.
- Что такое антибиотикорезистентность
- Вирусы и бактерии: в чем разница
- Как бактерии «учатся» противостоять антибиотикам: 4 основных механизма
- Цифры, которые должны насторожить
- Антибиотики против вирусов: почему это не работает
- Современные противовирусные препараты: стратегия разумной защиты
- Противовирусная защита: роль интерферонов
- Противовирусное средство при гриппе и ОРВИ
- Профилактика резистентности: что может сделать каждый
Что такое антибиотикорезистентность
Антибиотикорезистентность – это устойчивость бактерий к действию антибиотиков, при которой лекарственные препараты теряют способность уничтожать или подавлять рост микроорганизмов. Это явление возникает в результате естественного отбора: при неоправданном или неправильном применении антибактериальных средств выживают наиболее приспособленные штаммы, которые затем размножаются и передают гены устойчивости следующим поколениям[i].
Резистентность не означает, что организм человека стал невосприимчив к лечению – речь идет об изменении свойств самих бактерий. Микроорганизмы вырабатывают защитные механизмы: разрушают молекулы антибиотика ферментами, изменяют структуру мишеней, на которые направлено действие лекарства, снижают проницаемость клеточной стенки для препаратов или активно выводят их из клетки.
Последствия серьезны: инфекции, которые ранее легко излечивались, становятся опасными, увеличивается длительность госпитализации, растет потребность в дорогостоящих резервных лекарствах.
Профилактика резистентности – ответственность каждого. Антибиотики можно принимать только по назначению врача, строго соблюдая дозировку и продолжительность курса. Это помогает сохранить эффективность препаратов для будущих поколений и защищает от распространения «супербактерий», устойчивых к большинству известных антибиотиков[ii].
Вирусы и бактерии: в чем разница
Бактерии и вирусы часто объединяют в бытовом представлении как «микробы», однако их природа и механизм воздействия на человека фундаментально различны. Понимание этой разницы – основа грамотного подхода к лечению.
Бактерии – это самостоятельные одноклеточные организмы. Они имеют клеточную стенку, собственные системы обмена веществ и способны размножаться делением вне клеток хозяина. Патогенные бактерии вызывают заболевание двумя путями: выделяют токсины (как возбудитель столбняка) или заражают ткани, провоцируя воспалительный ответ (пневмококк, стафилококк). Иммунная система распознает бактериальные антигены и активирует фагоцитоз, выработку антител. Бактериальные инфекции часто сопровождаются гнойным отделяемым, локальным воспалением и хорошо поддаются лечению антибиотиками, которые разрушают клеточную стенку или блокируют синтез бактериальных белков.
Как действуют вирусы? Они устроены иначе: это генетический материал (ДНК или РНК) в белковой оболочке, не способный к самостоятельному размножению. Вирус проникает внутрь клетки человека, «перепрограммирует» ее метаболизм и заставляет производить новые вирусные частицы. Клетка-хозяин при этом гибнет. Так действуют вирусы гриппа в организме, герпеса, аденовирусы. Иммунный ответ на вирусную инфекцию включает выработку интерферонов – белков, блокирующих репликацию вируса, и активацию Т-киллеров, уничтожающих зараженные клетки. Антибиотики на вирус в организме не действуют: у вируса нет мишеней для этих препаратов.
Сколько вирусов в организме человека? В организме человека триллионы вирусов, но подавляющее большинство из них – нейтральные или полезные сожители, а не возбудители болезней. В их число входят бактериофаги – особые вирусы, поражающие бактериальные клетки и являющиеся компонентами здоровой микробиоты.
Ключевые отличия вирусов и бактерий в организме:
- вирусные инфекции часто начинаются остро, с лихорадки, ломоты, катаральных явлений;
- бактериальные осложнения обычно присоединяются позже, характеризуются гнойным отделяемым, длительной температурой;
- в организме вирусы вызывают системные признаки, бактерии – чаще локальные очаги воспаления.
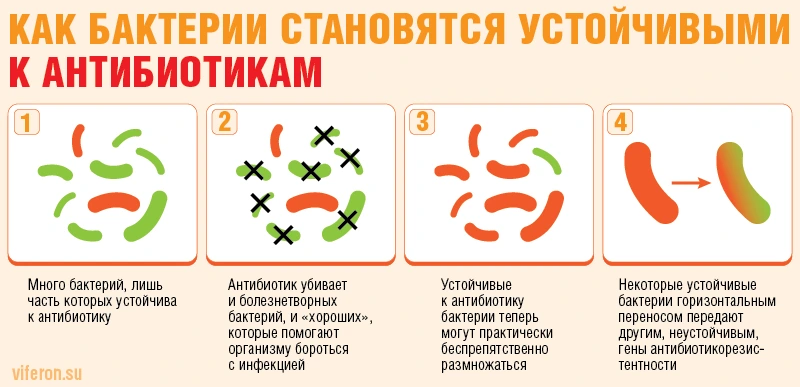
Как бактерии «учатся» противостоять антибиотикам: 4 основных механизма
Бактерии – настоящие мастера выживания. Резистентность становится результатом естественного отбора, который значительно усиливается неправильным применением лекарств. Ученые выделяют четыре ключевых механизма, благодаря которым бактерии становятся неуязвимыми.
Первый – ферментативная инактивация. Бактерии производят специальные ферменты, например бета-лактамазы, работающие как молекулярные ножницы. Они изменяют молекулы антибиотика до того, как препарат окажет эффект. Лекарство становится бесполезным еще до начала действия.
Второй способ – изменение мишени, на которые действует лекарство. Антибиотики атакуют конкретные структуры бактериальной клетки: клеточную стенку или ферменты, позволяющие бактериям синтезировать свои белки. Бактерия мутирует, форма мишени меняется. Препарат больше не может «узнать» цель и связаться с ней, словно ключ, переставший подходить к замку.
Третий механизм – снижение проницаемости оболочки. У бактерий есть внешняя мембрана с порами для проникновения веществ. Микроорганизм уменьшает количество пор или меняет их структуру. Двери закрываются, и антибиотик физически не попадает внутрь клетки в нужной концентрации.
Четвертый метод – активное выведение. В мембране работают насосы-эффлюксы. Лекарство проникает внутрь, но система распознает чужака и выталкивает его обратно. Концентрация препарата падает.
Бактерии обмениваются между собой информацией при помощи особых молекул ДНК – плазмид. Плазмиды содержат гены, которые повышают устойчивость бактерий к антимикробным препаратам и благодаря им устойчивость одного штамма быстро передается другому виду. Так локальная проблема превращается в глобальную эпидемию неуязвимых инфекций.
Из этого можно сделать вывод, что резистентность – естественный эволюционный процесс, но нерациональное использование антибиотиков ускоряет его в разы. Например, пациент не завершил полный рекомендованный курс, так как почувствовал себя лучше – в результате основная часть бактерий погибла, но остались «недобитые», которые пережили лечение и дальше оставили также устойчивое потомство.
Недостаточные дозы антибиотиков не оказывают терапевтического эффекта, но могут способствовать мутациям или переносу генов устойчивости плазмидами. Таким образом, каждый необоснованный или неправильно проведенный курс лечения создает полигон для отбора самых опасных штаммов.
Что такое биопленки?
70% инфекций сопровождаются формированием так называемых биопленок. Биопленки – это организованные сообщества бактерий и других микроорганизмов, которые прикрепляются к поверхностям (слизистым, зубам, имплантам, ранам) и окружают себя защитным слоем. Этот слой, или матрикс, бактерии создают сами из специальных веществ: сахаров, белков и фрагментов ДНК. Бактерии в биопленках становятся труднодоступными для иммунной защиты и действия антибиотиков. Бактерии в биопленках остаются живыми даже в присутствии антибиотиков, добавленных в количестве 500-1000 раз большем, чем их минимальная подавляющая концентрация[iii].
Именно поэтому инфекции, связанные с биопленками, часто приобретают хроническое течение и рецидивируют даже после курсов терапии. Разрушение матрикса и поддержка местного иммунитета слизистых оболочек становятся ключевыми условиями для успешного лечения таких состояний.

Цифры, которые должны насторожить
Проблема антибиотикорезистентности – угроза глобальной безопасности. По прогнозам ВОЗ, через 20-25 лет устойчивые инфекции могут уносить миллионы жизней ежегодно. Роспотребнадзор постоянно фиксирует рост числа штаммов, неподдающихся терапии. Особую тревогу вызывают метициллин-резистентный золотистый стафилококк (MRSA) и резистентные формы туберкулеза, лечение которых требует огромных ресурсов и времени.
Экономические последствия этой эпидемии не менее тревожны, чем медицинские. Пациенты с устойчивыми инфекциями вынуждены дольше оставаться в стационарах, что увеличивает нагрузку на медицинский персонал и требует применения дорогостоящих резервных препаратов. В результате стоимость лечения возрастает в разы, а риск развития тяжелых послеоперационных осложнений становится фактором, с которым приходится считаться при планировании любой хирургической помощи.
В России ситуация имеет свои особенности, во многом обусловленные исторически сложившейся культурой самолечения. Долгое время антибиотики находились в свободном доступе, что сформировало у населения привычку принимать их бесконтрольно – при первых признаках простуды, без назначения врача и часто с прерыванием курса. Такая практика создает идеальные условия для естественного отбора: выживают и размножаются именно те бактерии, которые смогли приспособиться к действию лекарств.
Что может сделать обычный человек в этой непростой ситуации? Все начинается с осознанного подхода: важно понимать, когда антибиотики действительно необходимы, а когда их применение не только бесполезно, но и потенциально опасно. Назначать лечение с применением антибиотиков может только врач.
Антибиотики против вирусов: почему это не работает
Когда антибактериальный препарат назначается при вирусной инфекции, он не просто «не срабатывает» – он запускает цепочку нежелательных процессов в организме.
Первый удар принимает на себя микробиом – полезные бактерии кишечника, кожи и слизистых оболочек. Они гибнут под действием препарата, предназначенного для борьбы с патогенами. Это нарушает естественный защитный барьер, снижает местный иммунитет и может спровоцировать дисбактериоз, грибковые инфекции или диарею. Восстановление микрофлоры требует времени и дополнительных усилий.
Кроме того, любой лекарственный препарат несет риск побочных эффектов – от аллергических реакций до нагрузки на печень и почки. Получая эти риски без малейшей терапевтической пользы, пациент подвергает организм неоправданной опасности.
Не менее коварна психологическая ловушка: создается иллюзия активного лечения, хотя реальная причина болезни остается без внимания, вирусы далее размножаются в организме. Время уходит, симптомы могут нарастать, а правильная тактика – противовирусная поддержка и симптоматическая помощь – откладывается.
Таким образом, применение антибактериальных средств при вирусе герпеса в организме, простуде и гриппе – это не нейтральная ошибка, а действие с отсроченными негативными последствиями. Разумный подход начинается с понимания: антибиотик спасает жизнь при бактериальной инфекции, но становится фактором риска, если используется не по назначению[iv].
Современные противовирусные препараты: стратегия разумной защиты
Разработка лекарств, способных победить вирус, – одна из сложнейших задач современной фармакологии. Создать препарат, который уничтожит возбудителя, но не повредит здоровые ткани, крайне трудно. Именно поэтому арсенал противовирусных средств с прямым действием остается довольно узким, требуя от врача и пациента стратегического подхода к лечению.
Прямое противовирусное действие: узкий арсенал
На сегодняшний день существуют препараты с доказанной эффективностью лишь для ограниченного круга возбудителей. Это лекарства, настроенные на конкретные молекулярные мишени. Например, для вируса гриппа применяются ингибиторы нейраминидазы. Они блокируют выход новых вирусных частиц из зараженной клетки, предотвращая распространение инфекции. Сколько вирус живет в организме? Некоторые вирусы живут недолго, как например, вирус гриппа, а другие – такие как герпесвирусы, способны пожизненно персистировать в организме человека.
Для вирусов герпеса разработаны аналоги нуклеозидов, которые встраиваются в цепочку ДНК возбудителя, обрывая его размножение. Такие средства позволяют сократить продолжительность эпизода, но не предотвращают развитие рецидива. Отдельного упоминания заслуживает антиретровирусная терапия для ВИЧ и препараты прямого действия для гепатитов В и С. Это яркие примеры успеха науки, позволяющие перевести хронические инфекции в контролируемое состояние, хотя часто требуют длительного или пожизненного приема.
Однако большая проблема заключается в том, что для большинства возбудителей острых респираторных инфекций – риновирусов, аденовирусов, РС-вируса – узконаправленных препаратов попросту не существует.
Ряд отечественных противовирусных препаратов, которые обладают широким спектром противовирусной активности и могут применяться при различных видах ОРВИ и других вирусных инфекциях, помогают сохранять здоровье взрослым и детям.
Противовирусная защита: роль интерферонов
В условиях отсутствия прямых лекарств для многих ОРВИ стратегия смещается в сторону поддержки иммунитета при вирусных инфекциях и выбора средств с широким спектром действия. Поскольку специфических лекарств против возбудителя не существует, на помощь приходит врожденный иммунитет. Ключевые игроки здесь – интерфероны. Это сигнальные белки, которые клетки организма экстренно вырабатывают в ответ на вирусную атаку. Они представляют собой первую линию обороны, запускающую защитные реакции еще до формирования специфических антител.
Механизм действия уникален. Интерфероны не атакуют вирус напрямую. Они активируют ферменты, блокирующие синтез вирусных белков в пораженной клетке. Кроме того, они связываются с рецепторами соседних незараженных клеток, предупреждая их об опасности, и те тоже начинают вырабатывать противовирусные ферменты. Одновременно интерфероны оказывают иммуномодулирующее действие – они помогают клеткам иммунной системы распознавать патогены и активируют макрофаги и натуральные киллеры, чья задача – уничтожать зараженные клетки.
Преимущества этих препаратов очевидны. Широкий спектр активности позволяет применять их при неидентифицированном возбудителе, что критично при ОРВИ. Иммуномодулирующий эффект помогает восстановить защитные силы без лишней нагрузки на организм.
Существуют различные формы выпуска лекарств, которые содержат интерфероны. Препараты в местных формах, например, в виде геля или мази, создают барьер во входных воротах инфекции и укрепляют местный иммунитет. Ректальные суппозитории обеспечивают системное действие без нагрузки на желудок. Важный нюанс: эффективность максимальна при раннем применении. Запускать защиту целесообразно в первые 48 часов, пока вирус не размножился.
Противовирусное средство при гриппе и ОРВИ
Одним из препаратов, способствующих укреплению иммунной системы и подавлению репликации вирусов, является противовирусный препарат ВИФЕРОН.
Он содержит рекомбинантный интерферон альфа-2b, который препятствует синтезу вирусных РНК и ДНК и блокирует размножение вируса.
Препарат был разработан в результате фундаментальных исследований в области иммунологии и выпускается в виде свечей, геля и мази. Уникальной особенностью препарата ВИФЕРОН является наличие высокоактивных антиоксидантов (витаминов С и Е), в присутствии которых противовирусное действие интерферона значительно усиливается. Несмотря на то, что препарат ВИФЕРОН широко известен как средство для лечения вирусных инфекций, он также применяется и в комплексной терапии бактериальных заболеваний, в сочетании с антибиотикотерапией. Иммуномодулирующие свойства ВИФЕРОН позволяют ему эффективно применяться при таких заболеваниях как как ОРВИ, осложненные бактериальной инфекцией, урогенитальные инфекции (хламидиоз, уреаплазмоз, трихомониаз, гарднереллез, бактериальный вагиноз, микоплазмоз). Также в этот список входят бактериальный простатит, инфекционно-воспалительные заболевания новорожденных (бактериальная пневмония, бактериальный менингит).
ВИФЕРОН обладает опосредованной антибактериальной активностью – помогает клеткам иммунной системы (фагоцитам и цитотоксическим лимфоцитам) уничтожать бактерии и поражённые ими клетки. Таким образом, он может применяться совместно с антибиотиками, позволяет снизить их терапевтические дозы и уменьшить токсические эффекты.
Кроме того, ВИФЕРОН способствует восстановлению местного иммунитета слизистых оболочек за счет повышения уровня факторов их защиты – секреторного иммуноглобулина А и интерферона. А это, в свою очередь, препятствует формированию и расселению на слизистых оболочках полимикробных биопленок, что также повышает эффективность комплексной терапии.
Профилактика резистентности: что может сделать каждый
- Вакцинация – первый рубеж обороны. Своевременная прививка от гриппа или пневмококковой инфекции снижает риск заболеть в принципе. Меньше заболевших – меньше назначений антибиотиков. Чем реже мы используем эти препараты, тем дольше они сохраняют свою эффективность.
- Гигиена как наука. Казалось бы, банальное мытье рук после улицы и респираторный этикет (чихать в локоть, использовать маски в сезон ОРВИ) разрывают цепочки передачи инфекций. Не позволяя бактериям путешествовать от человека к человеку, мы снижаем общую нагрузку на иммунитет и сокращаем потребность в лекарствах.
- Ответственное самолечение: табу на «остатки». Самое вредное, что можно сделать – это требовать у врача рецепт «на всякий случай» или начинать пить антибиотики, оставшиеся с прошлого раза.
- Поддержка микробиома. Здоровый кишечник – это огромная армия полезных бактерий, которые сами по себе защищают нас от патогенов. Рациональное питание с достаточным количеством клетчатки укрепляет эту защиту. Если же курса антибиотиков избежать не удалось, по рекомендации врача стоит подключить пробиотики, чтобы восстановить внутреннюю экосистему.
- Просвещение – наше все. Поделитесь этими знаниями с пожилыми родственниками, которые часто верят в «волшебную таблетку» в виде антибиотика. Дружеский разговор о вреде самолечения может сработать лучше строгих запретов.
Коллективный иммунитет к необоснованному применению антибиотиков – это не фантастика, а достижимая цель. Наш общий осознанный подход к здоровью сохранит лекарства эффективными для нас и наших детей.
Справочно-информационный материал
Автор статьи
Врач-терапевт, кардиолог, к.м.н.
Источники:
[i] https://cyberleninka.ru/
[ii] https://sciencejournals.ru/
[iii] Петухова И.Н., Дмитриева Н.В., Григорьевская З.В., Багирова Н.С., Терещенко И.В. Инфекции, связанные с образованием биопленок. Злокачественные опухоли 2019; 3s1:26–31.
[iv] https://cmac-journal.ru/