Локшина Э.Э., Зайцева О.В., Мазанкова Л.Н., Чеботарева Т.А., Коровина Н.А., Курбанова Х.И.2, Малиновская В.В., Гусева Т.С., Паршина О.В.
Кафедра педиатрии ГОУ ВПО МГМСУ Минздавсоцразвития России.
Кафедра детских инфекционных болезней с курсом детской дерматовенерологии ГОУ ДПО РМАПО Росздрава.
ФГБУ «НИИЭМ им. Н.Ф. Гамалеи» Минздравсоцразвития России.
В настоящее время острые респираторные вирусные инфекции (ОРВИ) являются наиболее массовыми инфекционными заболеваниями, у детей в возрасте до 5 лет занимают 70-90% от общей структуры заболеваемости. Дети в возрасте от 1 года до 5 лет чаще болеют ОРВИ, что объясняется постепенной утратой иммунитета, приобретенного от матери и несовершенством собственной иммунной защитной системы. Кроме того, известно, что у детей, находящихся в организованных детских коллективах (детские сады) ОРВИ возникают в среднем 8-10 раз на первом году посещения, 5-6 раз на втором, 3-4 раза на третьем.
Рассматривая вопросы распространенности острых респираторных заболеваний у детей, необходимо помнить об особенностях врожденного и адаптивного иммунитета. Это обусловлено Th2 направленностью иммунного ответа, несостоятельностью макрофагально-фагоцитарного звена, возрастными особенностями функционирования системы интерферонов (ИФН), снижением концентрации компонентов комплемента при альтернативном пути воспаления и продукции иммуноглобулинов классов G и A, незрелостью Т- и В-лимфоцитов [1-3]. Более частым эпизодам ОРИ у детей раннего возраста по сравнению со взрослыми способствуют анатомо-физиологические особенности дыхательной системы, прежде всего мукоцилиарной и сурфактантной системы, особенности строения бронхов.
Для системы интерферонов также характерны возрастные особенности. По мере развития ребенка происходит поэтапное созревание системы ИФН. Однако синтез ИФН у детей, особенно раннего возраста, значительно снижен по сравнению с таковым у взрослых. Поэтому несовершенство иммунитета и нейроэндокринной регуляции может приводить к повышенной восприимчивости к инфекционным заболеваниям, а также увеличивать частоту и тяжесть ОРИ. Кроме того, и другие факторы способны оказывать влияние на изменения в интерфероногенезе, такие как, нарушение питания, загрязнение окружающей среды, воздействие радиации. У часто болеющих детей, находящихся на искусственном вскармливании, живущих в условиях повышенной радиации, а также подвергшихся внутриутробному или постнатальному инфицированию снижена способность лейкоцитов к продукции ИФН. Воздействие экопатогенных факторов может приводить к сенсибилизации детского организма, существенно снижая его резистентность к вирусным и бактериальным инфекциям [4].
ОРВИ, имея разную этиологию, схожи по эпидемиологии, патогенезу и имеют общую симптоматику, требуют терапии до идентификации возбудителей и в этом случае важная роль отводится средствам, влияющим на иммунную систему и повышающим неспецифическую резистентность организма, а так же обладающим широким спектром действия на многочисленные возбудители ОРВИ. К этой группе препаратов относятся интерфероны.
Интерфероны (ИФН) – естественные цитокины, обладающие универсальными антивирусными свойствами: способностью к подавлению репликации многих РНК и ДНК– содержащих вирусов благодаря ингибированию процессов транскрипции и трансляции вирусных матриц. Кроме того, ИФН являются медиаторами иммунитета, повышают эффективность неспецифических защитных реакций: усиливают цитотоксичность сенсибилизированных лимфоцитов и NK–клеток, активность макрофагов, а также способствуют восстановлению нарушенного гомеостаза и оказывают иммуномодулирующее действие.
Из препаратов ИФН для лечения и профилактики ОРВИ у детей наиболее широко применяется лекарственное средство ВИФЕРОН, мазь, который представляет собой комплексный препарат интерферона человеческого рекомбинантного ?2, с токоферола ацетатом на основе ланолина безводного и вазелина медицинского. Содержание интерферона в 1г мази — 40000 МЕ.
В ряде случаев местное применение препаратов интерферона даже более эффективно, чем системное, так как позволяет добиться активации мукоцилиарных факторов защиты при меньшем расходе препарата. При введении препарата в носовые ходы, ВИФЕРОН действует в месте первичного внедрения и размножения респираторных вирусов на эпителиальные клетки слизистой оболочки носа.
Для оценки безопасности, переносимости и лечебной эффективности препарата ВИФЕРОН, мазь (Интерферон человеческий рекомбинантный альфа -2) при лечении ОРВИ и гриппа у детей нами было проведено мультицентровое рандомизированное двойное слепое плацебо контролируемое клиническое исследование.
Материалы и методы
Работа осуществлялась в эпидсезон 2007 — 2008 гг на трех клинических базах: кафедра педиатрии ГОУ ВПО МГМСУ Минздавсоцразвития России (Детская Городская Клиническая Больница Святого Владимира) под руководством проф. О.В. Зайцевой, кафедра детских инфекционных болезней с курсом детской дерматовенерологии ГОУ ДПО РМАПО Росздрава (проф. Мазанкова Л.Н.) и кафедра педиатрии ГОУ ДПО РМАПО Росздрава (проф. Коровина Н.А.) на базе отделений Тушинской детской городской больницы. Исследование проводилось в строгом соответствии с требованиями Хельсинской декларации (WMA, 1964) и «Декларации о политике в области обеспечения прав пациентов в Европе» (WHO/EURO, 1994).
Рандомизировано 100 детей в возрасте от 1 года и до 9 лет 10 месяцев, из них 65 (65%) мальчиков и 35 (35%) девочек. В возрастной структуре обследованных пациентов преобладали дети младшего возраста (от 1 года до 3 лет — 69%), дети от 3 до 7 лет составили 28%, и старше 7 лет – 3%.
Критериями включения в исследование были: пациенты с клинически установленным диагнозом острая респираторная вирусная инфекция или грипп; форма тяжести заболевания: среднетяжелая; госпитализация не позднее 48 часов с момента заболевания; возраст от 1 до 18 лет; информированное согласие родителей пациента или уполномоченных лиц на участие в исследовании, лабораторное подтверждение диагноза респираторного вирусного заболевания с помощью ПЦР.
Критериями исключения из исследования были: наличие гиперчувствительности, аллергические реакции на компоненты препарата; наличие тяжелых сопутствующих заболеваний (сахарный диабет, туберкулез, хронические заболевания печени и почек, онкологические заболевания в любой стадии, ВИЧ); несоблюдение пациентом назначений врача; применение других иммуномодуляторов за 4 недели до начала исследования и в период исследования.
Распределение пациентов по группам осуществлялось методом случайной выборки. Группа А – получала препарат серии 233 (50 детей), группа Б – получала препарат серии 144 (50 детей). Группы наблюдаемых детей были сопоставимы. По внешнему виду препараты Виферон и плацебо не отличались, упаковка – баночка с мазью (12г) зашифрованы под разными номерами серий (233 и 144).
Этиологическая расшифровка ОРВИ проводилась методом ПЦР в лаборатории легионеллеза ГУ НИИЭМ им Н.Ф. Гамалеи РАМН. Обработку проб смывов со слизистой носа проводили с использованием наборов пробоподготовки «Проба-НК» производства фирмы «ДНК-Технология». Амплификацию и детекцию вирусной ДНК проводили с использованием интеркалирующего красителя SYBR-green на амплификаторе для проведения ПЦР в реальном времени ICycler IQ фирмы «Bio-Rad» (США). Содержание цитокинов, интерферонов и IgA определяли иммуноферментным методом (тест системы фирмы «Вектор – Бест» Новосибирск). Статистический анализ данных выполнялся с использованием пакета программ Statistica 6.1 (StatSoft, Inc., США).
Дети получали препарат Виферон или плацебо в следующих дозировках, в зависимости от возраста: детям от 1 года до 2-х лет 2500 МЕ 3 раза в день, от 2-х до 12 лет 2500 МЕ 4 раза в день, распределяя равномерно в оба носовых хода после промывания физиологическим раствором. Длительность терапии составила 5 дней.
Результаты исследования
Оценку эффективности проводили у 90 детей, полностью завершивших исследование. Критериями оценки терапевтической эффективности препарата являлись сроки и темпы обратного развития основных проявлений болезни: нормализация температуры, исчезновение симптомов интоксикации, респираторных симптомов, и общая длительность заболевания, частота и характер осложнений.
У всех детей отмечались проявления катарального воспаления в носоглотке (заложенность носа, ринит, признаки ларинготрахеита) в той или иной степени выраженности, у каждого второго – симптомы острого стеноза гортани, а в ряде случаев – признаки бронхита, иногда с развитием бронхообструктивного синдрома (БОС).
До начала лечения у детей рандомизированных групп для выявления этиологии ОРВИ были взяты смывы из носа.
Этиология заболевания была установлена у большинства наблюдавшихся детей на основе клинической интерпретации, обнаружения вирусов в смывах со слизистой носа методом ПЦР.
Таблица 1.
Этиологическая структура ОРВИ в наблюдаемых группах.
| Вирусы | Плацебо (46),N(%) | ВИФЕРОН (44),N(%) | Р в-п
По критерию Х2 |
| Аденовирус |
5(10,9) |
6(13,7) |
р›0,05 |
| Парагрипп |
4(8,7) |
0 |
р›0,05 |
| РС вирус |
9(19,6) |
3(6,8) |
р›0,05 |
| Риновирус |
7(6,5) |
3(6,8) |
р›0,05 |
| Недифференцированное ОРВИ |
9(15,2) |
6(13,6) |
р›0,05 |
| Микст инфекция |
18(39,1) |
26(59,1) |
р›0,05 |
| РС +Аденовирус |
1(5,5) |
6(23,1) |
р›0,05 |
| РС+Парагрипп |
5(27,8) |
1(3,8) |
р›0,05 |
| Парагрипп + аденовирус |
1(5,5) |
4(15,4) |
р›0,05 |
| РС +риновирус |
5(27,8) |
2(7,7) |
р›0,05 |
| Парагрипп +риновирус |
3(16,7) |
6(23,1) |
р›0,05 |
| РС+ Парагрипп+ аденовирус |
0 |
2(7,7) |
р›0,05 |
| Риновирус+РС+аденовирус |
0 |
3(11,5) |
р›0,05 |
| Парагрипп+риновирус+аденовирус |
3(16,7) |
2(7,7) |
р›0,05 |
По критерию Х2 различие не значимо.
Этиологическая структура представлена следующими возбудителями: аденовирус у 11 (12,9%), парагрипп – у 4 (4,7%), РС вирус – у 12 (14,1%), риновирус – 10 (11,8%), смешанная инфекция у 44 детей (51,8%) в различных сочетаниях. Доминировало участие РС вируса и аденовируса – преимущественно в сочетании друг с другом или с другими респираторными вирусами, при этом у 10 детей удалось выявить более 3 возбудителей.
Длительность лихорадки при течении ОРВИ составляла от 0 до 5 дней, в среднем по группам: ВИФЕРОН — 1,56±0,2 суток, плацебо – 1,82±0,2 суток (р›0,05). Отсутствие значимых различий влияния терапии на продолжительность лихорадки возможно связано с применением жаропонижающей терапией при повышении температуры выше 38,50С.
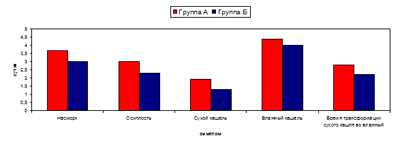
Выявлена тенденция к более быстрому купированию токсикоза у детей, получавших ВИФЕРОН: через 1-2 суток от начала лечения его проявления отсутствовали у 40,8% наблюдаемых, а в группе плацебо лишь у 10,4% (рРис. 1.
Средняя продолжительность катаральных симптомов в наблюдаемых группах.
*различие значимо (p‹0,05) по непараметрическому критерию Mann-Whytney
Для оценки противовирусного эффекта лечения оценивалась элиминация этиологически значимых вирусов в смывах из носоглотки после терапии. Анализируя данные нашего исследования было выявлено, что терапия человеческим рекомбинантным интерфероном альфа-2 в сочетании с – витамином Е имеет достоверные различия с препаратом плацебо в элиминации этиологических вирусов как при варианте моно, так и при варианте микстинфекции (таблица 3).
Полная элиминация вируса после лечения произошла в группе плацебо у 28,0% больных при моноинфекции, при микстинфекции у 55,5%, в группе, получавших Виферон у 91,6% и у 88,5%, соответственно, различия значимы (р‹0,05).
Таблица 2.
Влияние терапии на элиминацию различных респираторных вирусов из назальных смывов в наблюдаемых группах.
|
Вирус |
Количество пациентов (%) с элиминацией вируса на 5 день болезни |
|
|
Плацебо |
Виферон |
|
| Моноинфекция |
28 |
91,6# |
| Смешанная инфекция |
55,5 |
88,5# |
# различия значимы по Xi 2 p‹0,05
У части детей обеих групп при исследовании смывов из носоглотки после проведенной терапии отмечена контаминация дополнительными этиологически незначимыми вирусами, по – видимому, связанная с условиями пребывания детей в стационаре. Значительно реже регистрация «новых» вирусов отмечалась после терапии препаратом ВИФЕРОН — у 13 больных (29,5%), против 23 (50%) в группе плацебо (р‹0,05 по точному критерию Фишера) (табл. 4).
Таблица 4. Контаминация новыми клинически незначимыми вирусами
|
Вирус |
Количество пациентов (абс) с контаминацией новым вирусом на 5 день болезни |
Р п-в | |
|
Плацебо |
Виферон |
|
|
| Риновирус |
2 |
3 |
р›0,05 |
| Вирус парагриппа |
6 |
3 |
р›0,05 |
| РС-вирус |
3 |
3 |
р›0,05 |
| Аденовирус |
12 |
4 |
р‹0,05 |
| ИТОГО |
23 |
13 |
р‹0,05 |
различия значимы по Xi 2 p‹0,05
Выраженный протективный эффект против аденовируса выявлен у препарата Виферон, мазь контаминация данным вирусом происходила в 3 раза реже, чем в группе плацебо.
Для объективизации оценки иммунологической эффективности терапии с учетом сведений литературы о возрастных различиях интерфероногенеза и цитокиновых взаимодействий анализ проводился в двух возрастных подгруппах: от 1 года до 3 лет (n=61), старше 3 лет (n=29).
Диапазон иммунологических показателей у детей от 1 года до 3 лет до лечения в острый период заболевания составил ИФН – ? 2,8 – 29,5 пг/мл, ИФН – ? 0,1 – 8,56 пг/мл, ФНО — 8,26 – 323,9 пг/мл, ИЛ-8 — 3,38 – 2308,56 пг/мл, IgA- 3,7 – 11,4, что несколько отличалось от этих же показателей старшей возрастной группы.
Таблица 3.
Средние значения показателей интерферонового и цитокинового статуса до и после лечения у детей от 1 года до 3х лет.
|
Плацебо |
Виферон |
|||
| До лечения | После лечения | До лечения | После лечения | |
| ИФН — ? | 10,68±1,34 | 10,61±2,7 | 7,34±1,02 | 9,92±1,36 |
| ИФН — ? | 3,29±1,84 | 1,8±0,22 | 2,14±0,47 | 1,28±0,17 |
| ИЛ-8 | 384±85,36 | 366±125,8 | 416,2±73,61 | 291,4±71,03# |
| ФНО | 39,56±10,38 | 37,18±6,85 | 31,55±10,05 | 31,2±7,8 |
| IgA | 6,62±1,17 | 5,4±0,73 | 6,45±0,8 | 10,02±1,97#* |
# p‹0,05 непараметрический критерий Wilcoxon
* p‹0,05 непараметрический критерий Mann-Whytney
В процессе исследования показано, что влияние на показатели местного иммунитета в процессе лечения не было сильно выраженным. Тем не менее, ИФН – ? в группе детей, получавших ВИФЕРОН, повышался по сравнению со стартовыми значениями, в группе плацебо динамики отмечено не было. Средние значения ИФН – ? несколько снижались по сравнению с исходным уровнем, что характерно для детей с ОРВИ, причем более интенсивное снижение отмечено в группе плацебо. ИЛ-8 является активным участником острой воспалительной реакции, средние значения его снижались в 1,5 раза в группе ВИФЕРОНа после терапии, что свидетельствует о более быстром купировании местной воспалительной реакции на фоне проводимого лечения (p‹0,05). Средние значения ФНО существенно не изменились после лечения ни в одной из групп (таблица 5).
Значимое повышение среднего уровня секреторного IgA наблюдалось в группе ВИФЕРОНа после лечения с 6,45±0,8 мг/л до 10,02±1,97 мг/л (p‹0,05) и статистически значимо превалировал по сравнению с группой плацебо. Секреторный IgA является основным защитным фактором, препятствующим проникновению вирусов в эпителиальные клетки респираторного тракта, возможно, это объясняет протективный эффект лечения в отношении контаминации новыми вирусами в группе, получавших ВИФЕРОН, мазь.
В старшей возрастной группе достоверных различий в изменениях местного иммунитета получено не было (таблица 6).
Таблица 6. Средние значения показателей местного иммунитета у детей старше трех лет в наблюдаемых группах.
|
Плацебо |
ВИФЕРОН |
|||
| До лечения | После лечения | До лечения | После лечения | |
| ИФН — ? | 5,43±1,38 | 5,21±1,38 | 7,13±1,21 | 9,98±1,48# |
| ИФН — ? | 16,95±5,45 | 4,96±2,34# | 2,75±0,74 | 2,73±0,88 |
| ИЛ-8 | 526,41±269,53 | 564,89±270,03 | 945,5±233,96 | 420,68±128,13 |
| ФНО | 31,75±11,03 | 16,28±5,08 | 46,51±11,09 | 30,51±11,09 |
| IgA | 5,06±0,69 | 8,59±3,1 | 9,77±2,45 | 8,26±1,63 |
# p‹0,05 непараметрический критерий Wilcoxon
В группе Плацебо исходное среднее значение ИФН- ? было выше (16,95±5,45 пг/мл), чем в группе ВИФЕРОНа (2,75±0,74 пг/мл), в связи с этим сравнение динамики этого показателя оказалось некорректным.
Средние показатели ИЛ-8 до начала лечения в разгар заболевания были достаточно высокими (группа плацебо — 526,41±269,53 пг/мл, группа ВИФЕРОНа 945,5±233,96пг/мл). По окончании лечения в группе плацебо показатели практически не изменились (564,89±270,03 пг/мл), в группе ВИФЕРОНа отмечено существенное снижение (420,68±128,13 пг/мл), что может свидетельствовать об уменьшении воспалительного процесса.
Таким образом, учитывая результаты проведенного исследования, можно говорить о высокой эффективности человеческого рекомбинантного интерферона альфа-2 в сочетании с токоферолом. ВИФЕРОН оказывал положительное влияние на течение заболевания: уменьшалась продолжительность катаральных симптомов (сухого кашля), ускорялась трансформация сухого кашля во влажный, ускорялись темпы купирования токсикоза, темпы нормализации общего состояния. Отмечен выраженный противовирусный эффект, заключающийся как в элиминации этиологически значимых вирусов в смывах из носоглотки у большего процента больных (91,6% против 28%), так и в снижении контаминации «новыми» вирусами в группе детей, получавших ВИФЕРОН. Влияние на иммунологические параметры выявлено в исследовании тоже только в группе, получавших ВИФЕРОН, мазь — у детей в младшей возрастной группе от 1 года до 3 лет значимо повышался уровень секреторного IgA, а так же существенное снижение уровня ИЛ-8 в обеих возрастных группах.
Безопасность исследуемых препаратов учитывалась у всех больных, хотя бы раз получивших препарат. Критериями безопасности явились возникновение нежелательных явлений, серьезных нежелательных явлений, их связь с приемом препарата.
У 97% пациентов в целом применение препарата было признано безопасным. Наряду с этим, описан ряд нежелательных явлений у 4 детей (по 2 ребенка из каждой группы) (ринорея, чихание, жжение слизистой носа), топически соответствующий месту нанесения, и гиперемия слизистой носа в этой же области, оцениваемых во время терапии, по-видимому, связаны с основой, входящей в состав препарата. Достоверных различий при оценке данных нежелательных явлений в обеих группах не было.
Таким образом, результаты проведенного мультицентрового рандомизированного двойного слепого плацебо контролируемого клинического исследования подтверждают высокую терапевтическую эффективность и безопасность препарата ВИФЕРОН, мазь у детей раннего возраста, и позволяют рекомендовать использование препарата ВИФЕРОН, мазь в комплексной терапии ОРВИ и гриппа.
Литература:
1. Рачинский С.В.., Таточенко В.К. Болезни органов дыхания у детей: Руководство для врачей.- М. 1987.- 495 с.
2. «Инфекции респираторного тракта у детей раннего возраста» под ред проф. Г.А. Самсыгиной, 2006г, с.143
3. Макарова Светлана Альбертовна Клинико-функциональные особенности бронхообструктивного синдрома у детей раннего возраста и способы его коррекции Автореферат диссертации на соискание ученой степени к.м.н. 14.00.09 Год защиты: 2004 с. 17
4. Зайцева О.В. Препараты интерферона в повседневной практике врача. Медицинская кафедра, №3, 2002, с.50-55.
5. Нестерова И.В. Интерфероны в клинической практике. Труды XVI Российского национального конгресса «Человек и Лекарство» Москва, 6-10 апреля 2009, Том 1 , с.315-335.
6. Нестеров И.В. Препараты интерферона альфа в клинической практике. Российский Аллергологический журнал, №2, 2010. Стр.43-52
7. Ершов Ф.И., Григорян С.С., Орлова Т.Г. и др. Противовирусная терапия ОРВИ у детей.// Детские инфекции. 2006.- №3. – С.56-61.
8. Jefferson T.O., Tyerell D. Antivirals for the common cold. – Cochrane Database of Systematic Reviews 2005, Issue 3. – Published by John Wileyd@Sons Ltd., 2005.