Резюме
В настоящей статье дан обзор возможных вариантов лечения хронического вирусного гепатита С с генотипом 1в с использованием препарата «Виферон» и традиционной классической схемы лечения в сравнительной характеристике, на основе обзора побочных эффектов, первичного и стойкого ответа, а так же внешнесекреторной функции печени.
Гепатит С. Краткая характеристика. Эпидемиологическая обстановка.
В современный период в России имеет место резкая активизация эпидемического процесса гепатита С., начатая лишь в 1999 г. официальная регистрация впервые установленных случаев хронического вирусного гепатита С (ХВГС) выявила, что показатель за год вырос на 38,9%. В итоге за 2000г. лечебно-профилактическими учреждениями страны было выявлено и учтено 31 тыс. случаев острого ВГС, 156 тыс. случаев носительства возбудителя вирусного гепатита С и 32 тыс. случаев впервые установленного хронического ВГС. Частое поражение лиц молодого возраста, высокий уровень хронизации с возможным исходом в цирроз и первичный рак печени определяют повышенное внимание к этому заболеванию, актуальность и важность его дальнейшего изучения.
Вирус гепатита С в своей структуре неоднороден. К настоящему времени насчитывается до 34 генотипов вируса в одиннадцати генетических группах. Однако, принято выделять 5 наиболее общих генотипов, обозначаемых римскими цифрами I, II, III, IV и V, которые соответствуют генотипам la, lb, 2а, 2b и 3а.
На территории России частота встречаемости генотипов так же неоднородна. В Европейской части чаще других выявляются генотипы lb и 1а, а в Западной Сибири и на Дальнем Востоке — генотипы 2а и 3а.
У лиц с ХВГС, проживающих в московском регионе, преобладающим генотипом является lb (76%). Значительно реже обнаруживается генотип 1а (22%) и очень редко — генотип 3а (2%).
Большинство исследователей полагают, что с определенными генотипами HCV связаны различные исходы HCV-инфекции и неодинаковая эффективность интерферонотерапии при ХВГС.
В наблюдениях ряда авторов было установлено, что больные с ХВГС, обладающие генотипом lb HCV, более резистентны к интерферонотерапии, по сравнению с больными, имеющими генотипы 2а, 2b и другие.
Современный подход к лечению вирусного гепатита С
Внедрение препаратов интерферона альфа (ИФН?) в клиническую практику в середине 80-х гг. открыло новую эру в лечении вирусных гепатитов, позволив проводить этиотропную терапию этих болезней. Они представляют собой сочетание пептидов, которые синтезируются лимфоцитами и макрофагами. Название «интерферон» происходит от слова интерференция (взаимное влияние). В настоящее время препараты ИФН? являются самыми распространенными и наиболее изученными противовирусными агентами, применяемыми в лечении вирусных гепатитов.
Среди более чем 20 подтипов ИФН? наиболее биологически значимы альфа-2, рекомбинантными аналогами которого являются препараты Роферон (?2а), Интрон-А (?2b), а также отечественный Реаферон. Все выше перечисленные препараты обладают высокой эффективностью. Однако, препараты вводятся в организм больного парентеральным путем (внутривенно, внутримышечно, подкожно) и, как правило, в высоких дозах (3-10 млн. ME в сутки). При этом наблюдаются побочные эффекты: гриппоподобный синдром, сильные головные боли, артралгия, депрессивное состояние, галлюцинации, выпадение волос, диарея.
В результате фундаментальных исследований, проведенных в отделе интерферонов НИИ эпидемиологи и микробиологии им. Н.Ф. Гамалеи РАМН (Москва) под руководством профессора Малиновской В.В., была найдена реальная возможность обойти сложности, возникающие при парентеральном применении препаратов интерферонов. В процессе углубленных исследований функционирования системы интерферона в онтогенезе был выявлен ряд закономерностей, позволивший решить стоявшие перед разработчиками задачи: снижение дозировки интерферона при однократном его введении; пролонгирование действия интерферона; устранение побочных эффектов, характерных для парентерального введения препаратов интерферона; обеспечение возможности применения препаратов интерферона не только для лечения взрослых, но и в педиатрической (неонатологической) и акушерской практике. Результатом проведенной работы стал препарат Виферон, производимый в зависимости от дозы интерферона под номерами 1, 2, 3 и 4.
Выбранная лекарственная форма – суппозитории обеспечивает простой, безопасный и безболезненный способ введения, что особенно актуально для педиатрии (неонатологии), а также при амбулаторном лечении и самостоятельном приеме препарата больными.
В качестве действующего начала был выбран человеческий рекомбинантный ИФН-?2b один из наиболее распространенных в клинической практике. Кроме того, в состав Виферона помимо рекомбинантного ИФН-?2b, вошли мембрано-стабилизирующие препараты — антиоксиданты — ?-токоферола ацетат (витамин Е) и аскорбиновая кислота (витамин С) в терапевтически эффективных дозах.
Комбинированная терапия (КТ) ИФН с рибавирином в настоящее время является мировым стандартом в лечение HCV-инфекции.
Важно отметить, что свой противовирусный эффект при ХВГС рибавирин оказывает только в присутствии ИФН (монотерапия рибавирином неэффективна) и препятствует формированию резистентности вируса гепатита C к терапии. Хотя у 20-25% больных на фоне монотерапии рибавирином уровень трансаминаз нормализуется, после отмены препарата происходит возврат повышенных показателей АЛаТ и АСаТ.
Механизм действия рибавирина остается до конца не выясненным, хотя известно, что он является конкурентным ингибитором инозинмонофосфатдегидрогеназы. Рибавирин уменьшает внутриклеточный пул гуанозина трифосфата, что опосредованно сопровождается снижением синтеза вирусной РНК. Рибавирин способен избирательно накапливаться в моноцитах, лимфоцитах и эритроцитах, воздействуя таким образом на внепеченочные очаги HCV-инфекции.
Рандомизированное контролируемое исследование КТ рибавирина и ИФН в качестве первичной терапии HCV показало увеличение устойчивого ответа в 2 раза. Причем у пациентов с высокой репликативной активностью — более 3 млн. gE/мл – выявлено 10-кратное возрастание частоты постоянного ответа по сравнению с монотерапией ИФН (41 и 4% соответственно). У пациентов с низкой концентрацией вирусной РНК – менее 3 млн. gE/мл – не наблюдали преобладания эффективности КТ по сравнению с монотерапией ИФН. Частота постоянного ответа составляла 29% и 25% соответственно.
У больных HCV с исходно высоким уровнем виремии удлинение сроков КТ с 24 до 48 нед. на 10% увеличивает эффективность, тогда как у пациентов с низким уровнем виремии существенной разницы между эффективностью курсов выявлено не было.
При генотипе 1b КТ ИФН с рибавирином в течение 24-48 нед в 2-3 раза более эффективна, чем монотерапия ИФН. У пациентов с генотипом 1b 24-недельного курса КТ может быть достаточно в случае исходно низкого уровня виремии (менее 2 млн. gE/мл), а при уровне виремии более 2 млн. gE/мл требуется 48-недельный курс КТ. При других генотипах бывает достаточно 24-недельного курса КТ независимо от уровня виремии.
Немаловажным звеном в лечении ХВГС является применение озонотерапии (ОТ). При этом используется доказанный многими авторами выраженный антивирусный эффект, который проявляется как через непосредственное воздействие озона на вирус, так и опосредованно — через воздействие на вирус пероксидов, образующихся в результате взаимодействия озона с биологическими структурами организма, иммуномодулирующим действием озона. Важным оказывается и то, что озон стимулирует фагоцитоз, оказывает защитный эффект на здоровые клетки, в то же время повышая элиминацию клеток, пораженных вирусом.
Основным методом применения ОТ при гепатитах является внутривенное капельное введение 400 мл. озонированного физиологического раствора в дозировке 4-6 мг/л, несколькими процедурами в зависимости от формы ВГ. Различие в дозах при остром и хроническом гепатите связана с тем, что при этом используются различные механизмы действия ОТ. При остром гепатите необходимо антивирусное воздействие, а при хроническом важны иммуномодулирующий и протективный эффекты.
Материалы и методы исследования
На базе госпиталя № 1 Медслужбы МНТО «Гранит», было проведено лечение 82 человек больных ХВГС в стадии репликации. Из которых 45 мужчин и 37 женщин, средний возраст больных составил 33±1,8 лет. Из которых вирусный гепатит С с генотипом 1b был у 78 человек, 1а у 3 больных и 2а у 1 больного. Все больные были разделены на 4 группы. Длительность заболевания не превышала 5 лет, из всех обследованных лиц впервые выявленный ХВГС был у 27 человек, 19 обследованных получали ранее противовирусную терапию в виде монотерапии ?-интерферонами, длительностью не более 6 месяцев, первичный ответ был у 12 из этих больных. Уровень виремии у всех обследованных лиц составлял от 2 до 5 млн. gE/мл. Лица получавшие лечение ранее, были равномерно распределены в 2-ой, 3-ей и 4-ой группах. В первую группу вошли лица с впервые выявленным гепатитом, и лица с генотипами 1а и 2а.
Первая группа больных (17 человек) получала лечение в виде монотерапии Вифероном-4 в суточной дозировке 6 млн. МЕ на двухкратный приём через 12 часов, в течении 3-х месяцев, далее 3-х кратно в неделю, в течении 48 недель.
Вторая группа больных (24 человека) получала так же Виферон-4, по той же схеме, но в комбинации с Рибаверином (800-1200 мг суточной дозы)
Третья группа больных (16 человек) получала терапию Вифероном-4, Рибаверином (800-1200 мг суточной дозы) в сочетании с ОТ. ОТ проводилась путём внутривенного введения 400 мл озонированного физиологического раствора (с концентрацией О3 4-6 мг/л) в начале, в середине и в конце всего периода лечения курсами по 8 процедур, которые проводились 2 раза в неделю.
Четвёртая группа больных (23 человека) получала интерферонотерапию препаратом Реаферон в суточной дозе 6 млн. МЕ подкожного или внутримышечного введения ежедневно в течении месяца, далее трижды в неделю в течении 48 недель, в комбинации с Рибаверином (800-1200 мг).
Эффективность терапии оценивалась по первичному и стойкому ответу (исчезновение РНК ВГС и анти–ВГС-IgM, нормализация уровня АЛаТ и АСаТ). Кроме того, до и после 3-х месяцев от начала курса терапии была оценена внешнесекреторная функция печени путём проведения этапного хроматического дуоденального зондирования (ЭХДЗ).
Результаты исследования и их обсуждение
В ходе проведенного исследования были получены следующие результаты. Все больные прошли полный курс терапии (48 недель), прерывания курса лечения в связи с выраженными побочными эффектами не было, однако у некоторых больных в начале курса отмечались следующие симптомы.
Диаграмма 1
Побочные эффекты при лечении больных ХВГС (%)
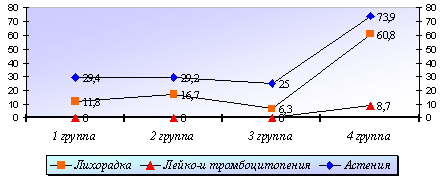
Как видно из диаграммы1 побочные эффекты в виде лихорадки и астенического синдрома наиболее часто встречались в 4-ой группе больных 60,8 и 73,9% соответственно. Минимальное проявление использованных схем лечения было в 3-й группе больных, получавшей Виферон-4, Рибаверин и ОТ, где лихорадка и астенический синдром были выявлены у 6,3 и 25% соответственно. В 1-ой и 2-ой группах побочных эффектов так же было отмечено немного, лихорадка и астенический синдром встречались в 11,8%, 16,7% и 29,4%, 29,2% случаев соответственно. Лейко и тромбоцитопении в 1-ой, 2-ой и 3-ей группах отмечено не было в отличие от группы больных получавшей парентеральные препараты интерферона, где умеренная лейко и тромбоцитопения были у 8,7% больных.
Оценка лечения проводилась с учетом первичного ответа (исчезновение РНК ВГС и анти–ВГС-IgM, нормализация уровня АЛаТ и АСаТ в конце лечения, зафиксированные не менее 2-х раз с интервалом не менее 2-х недель) и стойкого ответа (исчезновение РНК ВГС и анти–ВГС-IgM, нормализация уровня АЛаТ и АСаТ не менее 6 месяцев после окончания курса лечения). Результаты представлены на диаграмме 2.
Диаграмма 2
Ответ на лечение больных ХВГС (%)
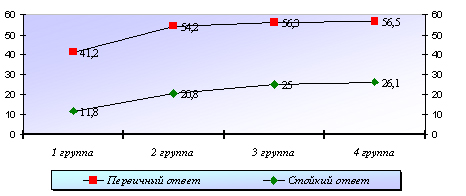
Как видно из диаграммы 2 максимальный терапевтический эффект был отмечен у больных, получавших лечение по 2-ой, 3-ей и 4-ой схемам, где стойкий эффект после проведённого курса лечения составил 20,8%, 25% и 26,1% соответственно, однако учитывая отсутствие достоверных отличий в стойком эффекте при использовании Реаферона в комбинации с Рибаверином и Виферона-4 в комбинации с Рибаверином и ОТ, и учитывая минимальные побочные эффекты в 2-ой и 3-ей группах больных следует отметить преимущество данных схем противовирусной терапии ХВГС.
При оценке внешнесекреторной функции печении путем проведения ЭХДЗ учитывалось наличие билиарной недостаточности (уменьшение количества желчи и желчных кислот, поступающих в кишечник за 1 час после введения раздражителя меньше 1,2 ммоль/час) результаты представлены в диаграмме 3.
Диаграмма 3
Снижение суммарного дебита холевой кислоты (билиарная недостаточность) у больных ХВГС (%)
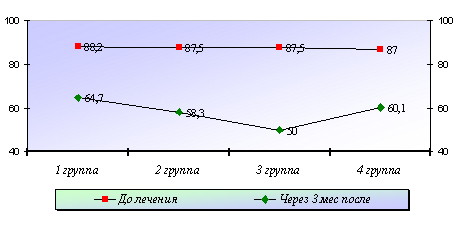
Как видно из диаграммы 3 при наличии приблизительно равной частоты встречаемости билиарной недостаточности (БН)у больных ХВГС от 87% до 88,2% обследованных больных до лечения, максимальный терапевтический эффект в коррекции БН отмечен у лиц получавших лечение по 3-ей схеме 50%, в отличии от 1-ой, 2-ой и 3-ей групп больных, где БН после лечения составляла 64,7%, 58,3% и 60,1% случаев соответственно, что говорит о преимуществе комбинации интерферона, Рибаверина с ОТ.
Таким образом, для лечения больных ХВГС целесообразно использование препаратов рекомбинатного ?2b интерферона в виде ректального суппозитория (Виферон-4) в комбинации с рибаверином и озонотерапией, что позволяет свести к минимуму возможные проявления побочных эффектов от инъекционной интерферонотерапии и добиться высоких показателей положительного ответа на лечение. Что, безусловно, позволяет расширить возможности лечения ХВГС у больных с сопутствующей патологией.
Кроме того, данная схема лечения позволяет максимально уменьшить явления билиарной недостаточности, что говорит об уменьшении литогенных свойств желчи, и снижении риска развития желчнокаменной болезни.
Заслуженный деятель науки России,
д.м.н., профессор Максимов В.А.
д.м.н., профессор Чернышев А.Л.,
к.м.н. Неронов В.А.
Межотраслевое научно-техническое объединение «Гранит».
НТЦ. Медслужба. Москва.