и эффективность виферонотерапии у детей с первичным гормоночувствительным нефротическим синдромом
А.А. Лындин 1, В.В. Длин 1, В.В. Малиновская 2, Е.А. Ружицкая 1, Шап Т.Г. 1, Т.С. Гусева 2, О.В. Паршина 2
1 ФГУ МНИИ педиатрии и детской хирургии Минздрава России, Москва
2 ФГУ НИИЭМ им.Н.Ф.Гамалея Минздрава России, Москва.
В статье представлен обзор, посвященный вирусассоциированному гломерулонефриту и показана эффективность включения в комплекс терапии детей с первичным гормоночувствительным нефротическим синдромом противовирусных и иммуномодулирующих препаратов, в частности, препарата Виферон®.
Наиболее частым иммунопатогенетическим механизмом развития гломерулонефрита (ГН) является иммунокомплексный и составляет 70-80% от общего числа больных ГН. В последние десятилетия, по мере развития новых технологий в изучении вирусной инфекции изменились представления о роли вирусов в патогенезе ГН [1,2,3]. Вирусассоциированным называется гломерулонефрит, при котором установлена этиологическая или патогенетическая роль вирусной инфекции.
В подавляющем большинстве случаев ассоциации ГН с НВ-вирусной инфекцией имело место бессимптомное или малосимптомное течение гепатита, проявляющееся преимущественно в виде изолированного повышения активности трансаминаз. Отмечена зависимость между клинической активностью ГН и титром антител вируса гепатита В (ВГВ), сероконверсией антител против НВеAg, а также уровнем специфических циркулирующих иммунных комплексов, содержанием антигенов ВГВ в почечной ткани [1,4,5].
Клинически и морфологически ГН, ассоциированный с НВ-вирусной инфекцией не отличается от клинических и морфологических вариантов ГН, при которых этот вирус не был обнаружен. В то же время, многими исследователями [1,6] отмечено, что для ГН, ассоциированного с НВ-вирусной инфекцией характерным является:
- высокая частота обострений;
- у большей части больных выявляется нефротический синдром со смешанным мочевым синдромом;
- заболевание чаще развивается у мальчиков в дошкольном возрасте;
- типичным является склонность к торпидному течению;
- характерен недостаточный ответ на стероидные и иммуносупрессивные препараты.
В последние 10-15 лет частота выявления маркеров ВГВ у детей с ГН снизилась на порядки и роль вирусов гепатита В как этиопатогенетического фактора при ГН резко снизилась в связи с внедрением прививок.
В отличие от этого, вирус гепатита С (ВГС) продолжает нередко выявляться у детей с тяжелыми формами ГН. После открытия в 1989 году ВГС и установления тесной связи смешанной криоглобулинемии с ВГС-вирусной инфекцией стала активно изучаться роль этого вируса в патогенезе ГН. Частота выявления смешанной криоглобулинемии среди больных с ВГС составляет 34-54% [7,8,9]. Смешанные криоглобулины состоят из иммуноглобулинов разных классов, чаще IgG и IgM со свойствами ревматоидного фактора – моноклонального IgМ? (II тип) и поликлонального IgМ (III тип). Наиболее высокой нефритогенностью обладает II тип [7]. Морфологически ГН, ассоциированный с ВГС, в том числе и протекающий с криоглобулинемией, близок к идиопатическому мезангиокапиллярному ГН.
Однако морфологические изменения в почках при криоглобулинемическом мезангиокапиллярном ГН имеют особенности, отличающие его от идиопатического мезангиокапиллярного ГН I типа:
• внутрикапиллярные тромбы, состоящие из преципитатов криоглобулинов и имеющие вид фибриллярных или кристаллоидных структур при электронной микроскопии;
• гиперклеточность клубочков из-за массивной инфильтрации лейкоцитами, главным образом моноцитов;
• выраженное удвоение и утолщение базальной мембраны клубочков почек;
• васкулит артерий мелкого и среднего калибра с участками фибриноидного некроза и моноцитарной инфильтрацией стенки.
Связь криоглобулинемического мезангиокапиллярного ГН с ВГС-вирусной инфекцией в дальнейшем была подтверждена и в исследованиях, проведенных в Европе (Италия, Франция, Испания), США и Японии. В настоящее время, выявляют структурные белки ВГС в иммунных отложениях в клубочке и интерстиции [10]. По данным Чумаковой О.В. (1999) [11] криоглобулинемия на +, ++ выявлялась у 44,4% детей с гломерулонефритом, ассоциированным с ВГС-вирусной инфекцией. Однако исследования проводились в условиях иммуносупрессивной терапии, что не исключает более высокие исходные показатели криоглобулинов у данных пациентов, и может служить косвенным подтверждением криоглобулинемического генеза почечного поражения. Клинико-лабораторные проявления ГН в сочетании с НС–вирусной инфекцией мало отличались от таковых при НВ-ассоциированном гломерулонефрите, и, в большей степени, отличались от ГН без поражения печени. При сочетании ГН с НС-вирусной инфекцией у большинства больных наряду с поражением почек и печени отмечались изменения со стороны других органов и систем (кожные сыпи, суставной синдром, поражение сердца, энцефалопатии, офтальмологические изменения) в разных комбинациях. Резистентность к стероидам была выявлена у всех детей при ГН в сочетании вирусом гепатита С [11].
Менее изучен вопрос о роли герпес-вирусной инфекции в этиологии и патогенезе ГН. Основная и наиболее характерная особенность этой группы вирусов – их способность к развитию латентной персистенции с присутствием вирусного генома. Инфекционный вирус образуется только в период эпизодов реактивации инфекции. Вирус обладает тропизмом к эпителиальным и нервным клеткам, кератотропен. Рецидивированию герпесной инфекции способствуют факторы, снижающие иммунную защиту, в частности интеркуррентные инфекции, особенно пневмококковая и вирусная, ультрафиолетовое облучение, гормональные изменения и иммуносупрессивные лекарства [12]. Защита организма против вируса простого герпеса (ВПГ) связана с клеточным иммунитетом, в первую очередь, с мононуклеарными клетками, которые участвуют в специфическом бластогенном ответе и антителозависимой цитотоксичности, а так же с естественными киллерными клетками. Гуморальный иммунитет не дает защиты против рецидивов инфекции [12].
Наиболее часто выявляют герпес-вирусы в биологических жидкостях (кровь, моча и/или слюна) методом культуральной диагностики или полимеразной цепной реакция (ПЦР). Исследуются антитела классов IgG и IgM к герпес-вирусам (цитомегаловирус, ВПГ, вирус Эпштейн-Барр) с помощью иммуноферментного анализа.
У детей с ГН имеет место высокая инфицированность вирусами, особенно из семейства Herpesviridae. ВПГ I типа определяется у половины больных с острым течением ГН, причем чаще он выявляется у детей с нефротическим синдромом (q=0,64), чем с нефритическим (q=0,2). Цитомегаловирусы (ЦМВ) и ВПГ II типа определяются очень редко у детей с остропротекающим ГН. ВПГ I типа чаще выделяется из крови, реже из мочи и лишь в единичных случаях – из слюны [13].
Существенным фактором, способствующим вирусной персистенции у больных ГН являются нарушения со стороны интерфероновой системы.
Исследования по изучению роли интерферонов при ГН в детских популяциях редки. Так при исследовании небольшой группы детей югославские авторы описывают снижение уровня индуцированной продукции ?-ИФН клетками периферической крови при рецидиве и на фоне стероидной терапии гормоночувствительного нефротического синдрома (ГЧНС), однако в ремиссии ГЧНС уровни индуцированного ?-ИФН не отличались от контрольных [14]. Об определенном снижении интерферонообразования у детей страдающих гломерулонефритом неоднократно отмечали и отечественные исследователи [1,2]. Так Длин В.В. (1993) [1] выявил достоверное снижение интерферонообразования у 83 детей страдающих различными формами гломерулонефрита, причем достоверных различий в зависимости от клинической формы гломерулонефрита не было получено. Изучение интерферонового статуса в 2 группах детей с гормонорезистентным нефротическим синдромом (ГРНС) и ГЧНС показало значительное снижение продукции ИФН-? и ИФН-? относительно нормативных показателей, при этом уровень сывороточного ИФН был повышен по сравнению с нормой. И хотя изменения были однотипны, в группе детей с ГРНС наблюдались достоверно более выраженные нарушения интерферонового статуса (ИФН-?, ИФН-?, сывороточный ИФН), по сравнению с детьми с ГЧНС [2].
Можно ожидать, что, когда имеет место участие вирусной инфекции в патогенезе гломерулонефрита, при эффективном использовании противовирусной терапии может наблюдаться улучшение со стороны течения и клинических проявлений гломерулонефрита. Гломерулонефрит ассоциированный с экстраренальными вирусными инфекциями, инициализируется обычно посредством сложных реакций компонентов иммунной системы. Так, например иммуноглобулины циркулирующих иммунных комплексов могут повреждать гломерулярные клетки при активации Fc рецепторов, но способствуют ли комплексы вирусных нуклеиновых кислот гломерулярному воспалению, остается неизвестным. Молекулярные патологические механизмы, посредством которых вирусные инфекции могут вызывать гломерулонефрит, остаются неясными [16, 17].
Лечение герпесвирусной инфекции до настоящего времени остается сложной задачей. Все разнообразие методов лечения и профилактики герпесвирусных инфекций, в конечном счете, сводится к трем главным подходам: иммунотерапии (препараты внутривенных иммуноглобулинов, интерферонов и вакцинации), химиотерапии (с применением препаратов аномальных нуклеозидов), либо к комбинации этих способов [18,19].
Современная противовирусная терапия эффективно уменьшает клинические проявления герпесвирусной инфекции, однако не предотвращает рецидивов заболевания [18]. В связи с этим предпринимаются попытки непосредственного воздействия на иммунную систему с целью стимуляции специфических и неспецифических ее факторов. В современной литературе трудно найти единое мнение по применению противовирусных препаратов в нефрологии, в частности при различных клинико-морфологических вариантах гломерулонефрита [1,13,18,20]. Учитывая вышеуказанные данные, можно полагать, что комбинированное применение противовирусных препаратов снизит частоту и интенсивность герпесвирусных инфекций, что, возможно, приведет к положительной динамике течения ГН.
Цель исследования: изучить состояние системы ?- и ?-интерферонов и оценить эффективность включения рекомбинантного ?2-интерферона (Виферон®) в комплекс лечения первичного гормоночувствительного синдрома.
Материалы и методы
Было обследовано 38 детей, страдающих первичным нефротическим синдромом (НС), в том числе 7 детей с дебютом нефротического синдрома, 8 – с рецидивирующим течением гормоночувствительного варианта нефротической формы гломерулонефрита, 23 – с гормонозависимым вариантом нефротической формы гломерулонефрита. Фильтрационная функция почек у всех пациентов была сохранна. Состав по полу был с преимущественным преобладанием мальчиков – 29 (76%), против 9 (24%) девочек. Возраст детей был от 2 до 17 лет, средний возраст составил 9,9±0,7 лет. Степень активности НС определялась согласно критериям по М.С. Игнатовой (1989) с изменениями [21]: активность ??? степени – выраженные отечный синдром, вплоть до анасарки, выраженные биохимические признаки НС (гипопротеинемия, гипоальбуминемия 25 г/л), протеинурия 30г/л, возможна остаточная гиперхолестеринемия), протеинурия менее 1г/сут; активность 0 степени – клинико-лабораторная ремиссия, отсутствуют экстраренальные, биохимические признаки НС, мочевого синдрома нет (белок в моче отсутствует).
Все пациенты по степени активности НС были разделены на 3 группы: в ? группу вошло 12 детей с активностью НС ??-??? степени, в том числе 8 мальчиков (67%) и 4 девочки (33%), средний возраст 9,9±1,3 лет; во ?? группу включено 20 детей с низкой активностью гормоночувствительного НС (? степени), в том числе 16 мальчиков (80%) и 4 девочки (20%), средний возраст 10,2±0,9 лет; ??? группа – 6 детей, находящихся в ремиссии НС более 4-х месяцев, в том числе 5 мальчиков (83%) и 1 девочка (17%), средний возраст 9,0±1,6 лет. Контрольную группу составили 8 практически здоровых детей, в том числе 6 мальчиков (75%) и 2 девочки (25%), средний возраст составил 8,78±0,86 лет. Таким образом, изучаемые группы по полу и возрасту достоверно не отличались (р>0,05).
Всем детям основных групп и группы контроля проводилось определение уровней ?-ИФНа и ?-ИФНа в сыворотке крови (в том числе сывороточный уровень и уровни спонтанной и индуцированной продукции). Для определения интерферонового статуса использовалась венозная кровь, постановку тестов производили в день забора крови. Инкубацию, разведенной средой крови, производили при 37°С в атмосфере 5% СО2 в течении 24 часов. Для индукции ?-ИФНа использовался раствор, содержащий вирус болезни Ньюкасла. Концентрацию ?-ИФН в сыворотке крови определяли иммуноферментным методом с применением наборов альфа-Интерферон-ИФА-БЕСТ (ЗАО Вектор-Бест, г.Новосибирск-117). Оценка результатов проводилась с помощью ИФА-анализатора «Antos-2020» (Австрия).
23 детям, принявшим участие в исследовании, и всем детям группы контроля проводилось исследование лейкоконцентрата крови и осадка мочи на наличие ЦМВ, Эпштейн-Барр вируса (ЭБВ), ВПГ методом ПЦР с применением соответствующих наборов «Herpes simplex virus 1 type», «Human cytomegalovirus», «Epstein-Barr virus» (НПФ «Гентех», Москва). Определение наличия антител класса М и G проводили с помощью ИФА с применением коммерческих иммуноферментных наборов тест-систем для выявлению соответствующих иммуноглобулинов НПО «Диагностические системы» (Москва).
Статистическая обработка полученных данных проводилась при помощи программы «STATISTICA 6.0». Проверка нормальности распределения осуществлялась с помощью критерия Колмогорова-Смирнова. При отличном от нормального распределения признаков, использовались непараметрические статистические методы. Изучение различий двух несвязанных групп проводилось с использованием критерия Манна-Уитни. Для определения корреляции применялся непараметрический коэффициент корреляции Спирмена. При проверке статистических гипотез наличие статистической значимости определялось при значении р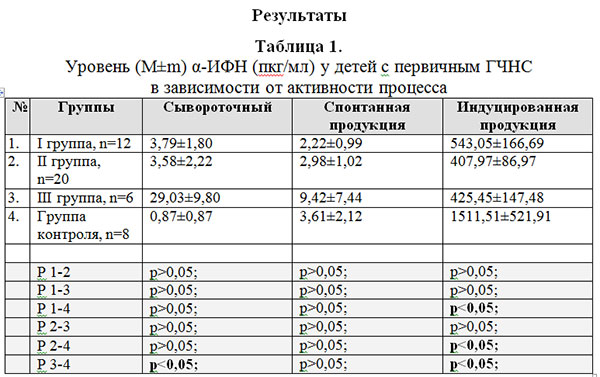
У детей с первичным ГЧНС независимо от активности процесса средний уровень сывороточного ?-ИФНа был выше по сравнению с группой контроля, но только у детей в ремиссии НС была достоверная разница (р0,05). Средний уровень индуцированной продукции ?-ИФНа у детей с первичным ГЧНС вне зависимости от активности НС был достоверно ниже чем в группе контроля (р0,05).
23 ребенка основной группы, которым проводилось вирусологическое обследование для выявления ЦМВ, ВПГ и ЭБ-вирусной инфекции методом ПЦР, были разделены на 4 группы: группу А составили 14 детей с отрицательными результатами определения ЦМВ, ВПГ, ЭБВ в крови и моче в том числе 11 мальчиков (79%), 3 девочки (21%), средний возраст 9,14±0,97 лет; группу Б – 9 детей с положительной реакцией хотя бы на один из определяемых герпес-вирусов в крови и/или моче, в том числе 5 мальчиков (56%) и 4 девочки (44%), средний возраст 6,72±0,95 лет; группа В – группа контроля составили 8 практически здоровых детей, в том числе 6 мальчиков (75%) и 2 девочки (25%), средний возраст 8,78±0,86 лет, все дети которой, имели отрицательные результаты определения ЦМВ, ВПГ, ЭБВ в крови и моче.
Независимо от установления факта инфицирования герпес-вирусными инфекциями (ВПГ, ЦМВ, ЭБВ) средний уровень сывороточного ?-ИФНа был выше чем в контрольной группе (табл. 2). Средний уровень спонтанной продукции ?-ИФНа достоверно не зависел от наличия персистирующей герпес-вирусной инфекции и не отличался от группы контроля. Средний уровень индуцированной продукции ?-ИФНа не зависел от наличия персистирующей герпес-вирусной инфекции, но был достоверно ниже, чем в группе контроля (табл. 2).
36 детей основной группы (2 ребенка из 38 выбыли из исследования по возрасту), были разделены на 2 группы: группу ? составили 18 детей, в том числе 13 мальчиков (72%), 5 девочки (28%), средний возраст 6,7±0,7 лет, которые в комплексной терапии НС получали препарат ?2-ИФНа (Виферон®) с противовирусной и иммуномодулирующей целями (1 суппозиторию 2 раза/сут с интервалом 12 часов в течение 10 дней ежедневно, затем – 3 раза в неделю через день в течение 4-6 месяцев (до 7 лет 150 тыс. МЕ 2 раза в день, старше 7 лет – 500 тыс. МЕ 2 раза в день). В группу ?? были включены 18 детей, в том числе 13 мальчиков (72%) и 5 девочек (28%), средний возраст 9,3±1,1 лет, не получавших препарат Виферон® в комплексной терапию НС. Дети обоих групп достоверно не отличались по проводимой патогенетической иммуносупрессивной терапии (глюкокортикоиды, хлорбутин, циклоспорин–А, мофетил микофенолата в стандартных дозировках).
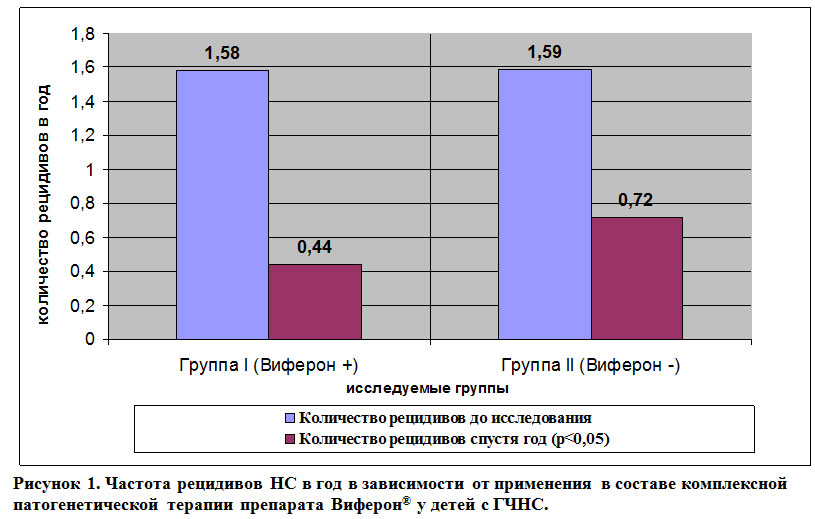
Среднее количество рецидивов НС до и после включения препарата Виферон® в группе ? составил 1,58±0,24 и 0,44±0,17 рецидива в год, соответственно. В группе без включения в терапию препарата Виферон® (группа ??) количество рецидивов НС до включения в исследование и спустя год наблюдения составило 1,59±0,26 и 0,72±0,21 рецидивов в год, соответственно (р® приводит к снижению частоты рецидивов НС, однако учитывая небольшое число исследуемых, трудно оценить различие влияния у детей с рецидивирующим ГЧНС и ГЗНС.
Таким образом у детей с ГЧНС, независимо от активности НС, отмечался более высокий уровень сывороточного ?-ИФНа и значительное снижение уровня индуцированного ?-ИФНа по сравнению с контрольной группой, что указывает на нарушение системы интерферона и ослабление противовирусной защиты и соответствует данным литературы [4,5]. У детей с выявленной персистенцией герпес-вирусов имеется тенденция к более низкому уровню спонтанной и индуцированной продукции ?-ИФНа.
Следует отметить, что аналогичные изменения интерферонового статуса, в виде повышения сывороточного ИФН и значительного снижения индуцированной продукции ИФН-? были показаны Лутошкиным И.В. (2005) [6] у детей с ГРНС.
Включение длительной, до 3-х месяцев виферонотерапии в комплекс лечения пациентов с ГЧНС ассоциированным с ГВИ позволяет снизить частоту рецидивов, что косвенно указывает на значение персистирующей вирусной инфекции в рецидивировании НС.
Список литературы:
1. Длин В.В. Патогенетическое значение персистирующей вирусной инфекции при гломерулонефрите у детей в обосновании противовирусной и иммуномодулирующей терапии // Дис……………док. мед. наук. М. 1993. 542с.
2. Лутошкин И.С. Персистирующая герпесвирусная инфекция у детей с гломерулонефритом // Росс. Вест. Перинат. Пед. 2005. Т.50. №4. С. 32-37.
3. Лындин А.А. Клинико-иммунологическая характеристика нефротической формы гломерулонефрита, ассоциированного с герпесвирусной инфекции у детей и повышение эффективности его лечения // Автореф. … дис. канд. мед. наук. М. 2012. 24 с.
4. Shin H.I. Clinicopathological study on membranous nephropathy in 16 children // Abstr. of 17 Intern. Congr. of Pediat.Manila. 1983. № 1. P. 139.
5. Zhang I.H., Li L-S., Zhon H. Is there a hepatitis B virus-associated glomerulonephritis? Identification of HBsAg, HBeAg and HBcAg in kidney with monoclonal antibodies // Chinese Medical J. 1989. Vol. 102. №7. P.496-504.
6. Nammalwar B.R., Sankar V.S., Ramesh S. et al. Hepatitis B virus infection and glomerulonephritis // Ind. I. Pediatr. 1987. Vol. 54. № 5. P. 759-763.
7. Козловская Л.В., Гордовская Н.Б., Малышко Е.Ю. и соавт. Криоглобулинемическое поражение почек: особенности течения и лечение // Нефрология и диализ. 2002. Т.4. №1. С.4-8.
8. Мухин Н.А., Козловская Л.В., Малышко Е.Ю. и соавт. Криоглобулинемический нефрит, ассоциированный с хронической инфекцией вируса гепатита С // Тер.архив. 2000. Т.6. С.1-5.
9. Agnello V., Romain P.L. Mixed cryoglobulinemia secondary to hepatitis C virus infection // Dis.Clin. North Am. 1996. Vol. 22. N1.
10. Sansonno D., Gesualdo L., Manno C. et al. Hepatitis C virus related proteins in kidney tissue from hepatitis C virus infected patients with cryoglobulinemic membranoproliferative glomerulonephritis // Hepatology. 1997. Vol.26. P.1687-1688.
11. Чумакова О.В. Особенности течения сочетанных болезней почек и печени // Дис……………док. мед. наук. М. 1999. 300с.
12. Leigh I.M. Management of non genital herpes simplex virus infections in immuno-competent patients // Amer.J. Med. 1988. Vol. 85. P.34-38.
13. Горчакова Л.Н. Роль герпес-вирусной инфекции в прогрессировании остропротекающего гломерулонефрита и обоснование использования альфа2–рекомбинантного интерферона // Автореф. дис… канд. мед. наук. М. 1999. 24 с.
14. Stefanovi? V., Golubovi? E., Miti?-Zlatkovi? M. et al. Interleukin-12 and interferon-gamma production in childhood idiopathic nephrotic syndrome // Pediatr Nephrol. 1998. Vol. 12. N 6. P. 463-466.
15. Лутошкин И.С. Клинико-патогенетическое значение и тактика лечения персистирующей герпесвирусной инфекции у детей с гормонорезистентным и гормоночувствительным вариантами нефротического синдрома. // Автореф. … дис. канд. мед. наук. М. 2005. 26 с.
16. H?gele H. Allam R., Pawar R.D. et al. Double-stranded RNA activates type I interferon secretion in glomerular endothelial cells via retinoic acid-inducible gene (RIG)-1 // Nephrol Dial Transplant. 2009. Vol. 24. N. 11. P. 3312-3318.
17. Allam R. Lichtnekert J., Moll A.G. et al.Viral RNA and DNA trigger common antiviral responses in mesangial cells // J Am Soc Nephrol. 2009. Vol. 20. N. 9. P. 1986-1996.
18. Малый В.П. (ред.). Герпесвирусная инфекция. М.: «Эксмо», 2009. 304 с.
19. Yu Z., Manickan E., Rouse B.T. Role of interferon-gamma in immunity to herpes simplex virus // J. Leukoc. Biol. 1996. N. 60. P. 528-532.
20. Зайцева О.В., Зайцева С.В. Лечение и профилактика острых респираторных инфекции у часто болеющих детей // Лечащий врач. 2008. №8. С. 53-57.
21. Таболин В.А., Бельмер С.В., Османов И.М. (под ред.). Нефрология детского возраста: практическое руководство по детским болезням. М.: «ИД Медпрактика-М», 2005. 712 с.