Мазанкова Л.Н., Чеботарева Т.А., Брагина Г.С.
ГОУ ДПО Российская медицинская академия последипломного образования Росздрава, Москва
ГУ НИИЭМ им. Н.Ф.Гамалеи РАМН, Москва.
На протяжении последних лет в России отмечается неуклонный рост заболеваемости ОКИ, составивший по данным Федерального центра Госсанэпиднадзора РФ в 2005г. — 1720 случаев на 100 тыс. детей, в 2006г. — 1768 случаев на 100 тыс. детей, а в 2007г. — 1790 на 100 тыс. детей в возрасте до 14 лет. Особенно высока заболеваемость ОКИ детей раннего возраста (до 70%). В современной этиологической структуре ОКИ ведущее место занимают вирусные диареи, составляя 50-70% всех случаев кишечных инфекций. Среди причин летальности у детей,связанной с инфекционной патологией, ОКИ стойко занимают второе место после острых респираторных инфекций.
В научной медицинской литературе широко представлены работы об этиологической структуре, патогенезе, клинических особенностях различных нозологических форм ОКИ, а также исследования по эффективности проводимого лечения [1,2]. Однако, до настоящего времени многие аспекты иммунопатогенеза ОКИ, в первую очередь вирусных диарей, изучены недостаточно. Нет однозначного мнения о выборе противовирусных, иммуномодулирующих препаратов при ОКИ разной этиологии.
В работах разных авторов представлены разноречивые данные о характере иммунных сдвигов и их влиянии на течение ОКИ. Так, при ОКИ бактериальной этиологии регистрируется снижение фагоцитарной активности нейтрофилов, уровня
IgM в сыворотке крови [3], при эшерихиозной инфекции у детей снижается число CD3, CD4 при повышении CD8 [4]. В то же время при кишечных инфекциях, вызванных условнопатогенными микроорганизмами, выявляется угнетение иммунорегуляторных клеток и высокое содержание IgМ при снижении уровня IgG [5]. У больных с ротавирусной инфекцией наряду с дефицитом CD3, CD4 отмечается снижение уровня IgА и фагоцитарного показателя в крови [6,7]. Показано, что при ОКИ различной этиологии у детей наступает депрессия местного иммунитета, снижение sIg A [8].
Развитие здоровой кишечной микрофлоры является ключевым фактором адекватной стимуляции, тренировки и созревания иммунной системы кишечника. Известно, что кишечная микрофлора, в частности, бифидобактерии, выполняет важные иммунные функции, способствуя синтезу факторов иммунной защиты (лизоцим, пропердин, комплемент, sIg A), активации фагоцитоза, стимуляции системы цитокинов и интерферонов [9, 17], что определяет иммунобиологический эффект при применении пробиотиков.
Нарушения местного и системного иммунитета при ОКИ у детей и большая роль нормальной микрофлоры в сохранении и коррекции иммунных параметров определяют актуальность поиска дополнительных путей совершенствования лечебной тактики при этих заболеваниях и послужили основанием для использования иммунных препаратов и пробиотиков.
Препараты интерферона (реаферон, реальдирон, велферон, лейкинферон и др.) наряду с положительным влиянием на динамику клинических проявлений, демонстрируют их противовирусный и иммуномодулирующий эффекты [10,18]. Однако способы их применения (инъекционный, ингаляционный) и частота побочных реакций ограничивают использование названных препаратов у детей, особенно раннего возраста.
Одним из широко применяемых в последние годы интерфероновых препаратов является «Виферон®» [11,12], содержащий в своем составе человеческий рекомбинантный ИФН ?-? и мембраностабилизирующие компоненты. Опыт его успешного использования при ряде вирусных, бактериальных и др. заболеваний – грипп, ОРВИ, острые и хронические гепатиты, герпес, ЦМВ-инфекция, дифтерия, хламидиоз и др. [13] и удобство лекарственной формы (свечи) позволили считать целесообразным применение Виферона у детей. Для обоснования рациональной тактики виферонотерапии ОКИ у детей необходимы дополнительные сведения об иммунном статусе при данной патологии, в частности, — особенности состояния системы интерферона и цитокинов в динамике при вирусных ОКИ у детей разного возраста, а также их клиническое значение. Уточнение особенности иммунопатогенеза ОКИ и оптимизация иммунотерапии в зависимости от характера изменения интерферонового статуса и цитокинов (Виферон, Бифиформ-«Малыш») являются актуальными аспектами изучения ОКИ на современном этапе. Целью настоящего исследования явилось изучение иммунологических аспектов развития ОКИ и совершенствование их терапии.
Материалы и методы. Работа проводилась в период с мая 2005 года по декабрь 2006 года на базе 4-го инфекционного отделения Тушинской детской городской больницы Департамента здравоохранения города Москвы [14]. Исследования иммунологических параметров проводились в лаборатории онтогенеза и коррекции системы интерфероногенеза НИИЭМ им. Н.Ф. Гамалеи и в лаборатории Центра иммунокоррекции НИИ трансплантологии и искусственных органов.
Было обследовано 145 больных с острыми кишечными инфекциями в возрасте от 5мес. до 14 лет, госпитализированных на 1-2-й день заболевания, у которых отсутствовали пищевая аллергия, лактазная недостаточность и в анамнезе на момент исследования отсутствовал факт приема пробиотиков и иммуномодуляторов. Идентификация этиологически значимых вирусов проводилась методами: ИФА для выявления ротавирусного антигена в кале с использованием иммуноферментной моноклональной тест-системы «Рота-анализ» и ПЦР.
Этиологическая структура ОКИ установлена у 81,4 % детей, в т.ч. у 76,6% выявлена вирусная этиология заболевания (ротавирусная инфекция 53,8%, норовирусная инфекция 9,7%, астровирусная инфекция 3,4%, mixt-вирусная инфекция 9,7%).
У 75,2% детей установлен осмотический тип диареи, этиологически ассоциированный преимущественно с рота- и норовирусами. У 8,3 % детей имел место инвазивный тип диареи, у 8,9 % отмечалась секреторная диарея, у 7,6% детей заболевание протекало без диареи. При всех типах диареи заболевание чаще протекало в среднетяжелой форме (80-92%).
Иммунологическое обследование проводилось в 1-2 день болезни и в периоде ранней реконвалесценции (5-6 день болезни). Исследовали уровни провоспалительных цитокинов (ИЛ-1?, ИЛ-6, ИЛ-8, ФНО-?, ИФН-?, ИФН-?) в сыворотке крови и способность к продукции ИКК ИФН-? и ИФН-? in vitro методом ИФА с набором реагентов BIOSOURSE (Бельгия), «Протеиновый контур» (СПб); параметры фагоцитарной активности нейтрофилов крови (фагоцитарное число, фагоцитарный индекс) с использованием убитой взвеси Staph. aureus по методу Петрова Р.В.; содержание иммноглобулинов А, М, G в сыворотке крови по методу Manchini G. et al.; концентрацию секреторного иммуноглобулина А в копрофильтратах методом радиальной иммунодиффузии по Manchini G. et al..
Проводилась оценка клинико-иммунологической эффективности комбинированного пробиотика «Бифиформ Малыш», содержащего в своем составе лактобациллы LGG, оказывающих выраженный противовирусный и иммунобиологический эффект (1 группа); рекомбинантного ?2b-интерферона Виферона в свечах, который является противовирусным и иммуномодулирующим препаратом (2 группа) и их комбинации (3 группа) в сравнении с контрольной группой. Группы были сопоставимы по возрасту, тяжести, особенностям клинической картины заболевания.
Статистический анализ данных проводился с использованием пакета программ STATISTICA 6.1 (StatSoft Inc., США).
Результаты исследования показали, что в острый период ОКИ независимо от типа диареи закономерно снижался уровень сывороточного иммуноглобулина А до 0,71г/л±0,45 при норме 0,93г/л±0,3 у 70,6% детей и повышался уровень Ig М до 1,3г/л ± 0,74 при норме 0,56г/л±0,2 в крови у 94,1% детей, что свидетельствует об активации антителообразования в первые дни заболевания на фоне повышения местного (секреторного) ответа на антигенную стимуляцию в кишечнике. При этом уровень иммуноглобулина G (8,55г/л±2,99) в начальный период заболевания у 94,1% больных был в пределах нормы.
У 77,8% детей выявлено снижение фагоцитарного индекса и у 100% детей — снижение в 1,5 раза фагоцитарного числа в первые дни заболевания. Так, средний показатель фагоцитарного индекса (%) составил 40[36-50], Ме[Q1; Q3] при норме 50-70; фагоцитарного числа (микробных тел) — 3[2,4-3,3], Ме[Q1; Q3] при норме 4-7.
При ротавирусной инфекции дефицит фагоцитоза у 81,6% больных коррелирует со слабой системной продукцией ИФН-? и -?, что обусловлено, вероятно, иммуносупрессивным действием вируса в остром периоде заболевания [6].
Проведен раздельный анализ продукции интерферонов (ИФН-? и -? в сыворотке, спонтанных и индуцированных) и провоспалительных интерлейкинов (ИЛ-1?, ФНО-?, Ил-6, ИЛ-8) — медиаторов клеточного иммунитета в результате которого показано, что в острый период ОКИ наиболее значимые изменения связаны с выраженной стимуляцией синтеза провоспалительного монокина ИЛ-1? – регулятора Тh-1 типа клеточного ответа. Выявлена корреляция между кратностью повышения ИЛ-1? и выраженностью лихорадки, эксикоза и кратности рвоты. Однако достоверного влияния уровня ИЛ-1? на тяжесть заболевания в целом не установлено.
Сравнительный анализ основных клинических симптомов ОКИ в зависимости от уровней ИЛ-1? и ИЛ-6 в крови выявил, что у 47,8% детей с повышенным уровнем ИЛ-1? и ИЛ-6 в крови отмечалась лихорадка выше 39,0?, что достоверно чаще, чем у детей с высоким уровнем ИЛ-1? и нормальным уровнем ИЛ-6 (р=0,013). У 69,6% детей с повышенным уровнем ИЛ-1? в сыворотке и нормальным уровнем ИЛ-6 заболевание протекало с лихорадкой до 38,0? (р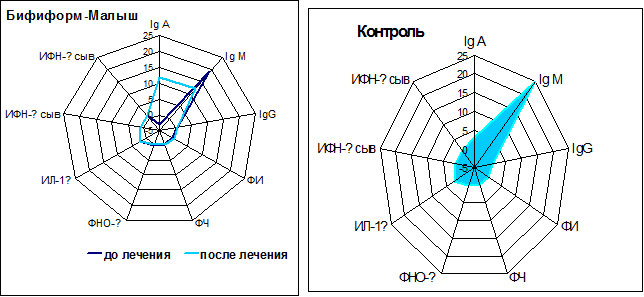
Виферон в острый период ОКИ оказывал положительное влияние на купирование симптомов интоксикации (р=0,047), сокращение длительности диареи и абдоминального синдрома на 0,4-0,6 дня. Уровни сывороточных и спонтанных ИФН-? и ИФН-? в обеих группах после лечения были в пределах нормы (0-50пкг/мл), а показатели индуцированных ?- и ?-ИФН — сниженными (менее 100пкг/мл и менее 1000пкг/мл соответственно). На фоне виферонотерапии в 2 раза повышался уровень ?- и ?-ИФН индуцированных у 37,5% и 46,1% детей соответственно, что превышало показатели контрольной группы. Достоверного влияния Виферона на интерфероногенез в острый период ОКИ не выявлено, что связано с низкой ?-интерфероноиндуцирующей способностью вирусов в первые дни заболевания [16].
При использовании в лечении ОКИ комбинации Виферона с пробиотиком «Бифиформ Малыш» получен достоверный клинико-иммунологический эффект: снижение в крови уровня провоспалительного ИЛ-6 (р=0,025), повышение уровня ИФН-? индуцированного до нормы у 66,7% детей, сокращение продолжительности интоксикации (р=0,001) по сравнению с монотерапией.
Проведенный сравнительный анализ наиболее показательных клинических симптомов в динамике по дням терапии позволил выявить преимущества каждого препарата (рис.2).
На фоне приема препарата «Бифиформ Малыш» у детей в более ранние сроки отмечалась нормализация стула (на 3-й день лечения диарея сохранялась только у 63,6% детей, при виферонотерапии — у 82,4% детей), длительность заболевания составила 5,06±0,96 дня.
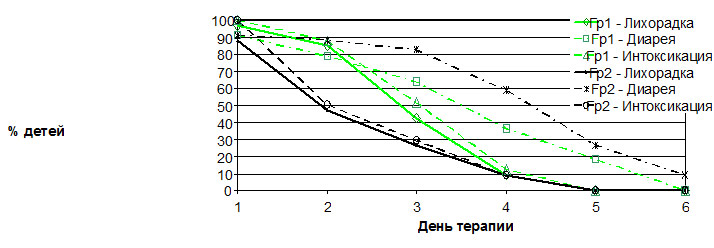
Рис. 2 Сравнительный анализ основных клинических симптомов по дням применения разной иммуномодулирующей терапии
У детей, которые получали Виферон в комплексной терапии ОКИ, быстрее, чем у детей контрольной группы, нормализовалась температура тела и исчезали симптомы интоксикации: на 2-й день терапии сохранялись лихорадка и симптомы интоксикации у 47,1% и 50,0% детей соответственно, а у детей 1 группы — у 84,8% и 87,9% детей. Заболевание длилось 5,20±1,49 дня.
На фоне комбинированной терапии на 2-й день от начала лечения только у 45,7% детей сохранялась лихорадка и у 48,6% детей симптомы интоксикации, на 3-й день — диарея у 65,7% детей. Длительность заболевания составила 5,07±1,2 дня.
Таким образом, у 91,8% детей с ОКИ независимо от типа диареи, тяжести и периода заболевания отмечается недостаточная продукция индуцированного альфа- и гамма — ИФН, а также снижение показателей активности фагоцитоза, что свидетельствует о качественном дефекте острофазного иммунного ответа и дефиците клеточного звена иммунитета.
При ротавирусной инфекции ключевым фактором иммуносупрессии является подавление продукции интерферонов, что сопровождается снижением показателей индуцированного ИФН-? и ИФН-? и является обоснованием к назначению в комплексе лечения иммунобиологических препаратов в острый период заболевания. Применение Виферона в комбинации с препаратом «Бифиформ Малыш» позволяет получить наряду с клиническим эффектом достоверное снижение в крови уровня провоспалительного ИЛ-6 (р=0,025) и повышение уровня индуцированного ИФН-? до нормы у 66,7% детей, что и определяет целесообразность применения комбинированной терапии в острый период вирусных диарей с исходно низким уровнем интерфероногенеза.
Список литературы:
1. Воротынцева Н.В., Мазанкова Л.Н. Острые кишечные инфекции у детей.-М.,Медицина,2001.- 480с.
2. Учайкин В.Ф., Мазанкова Л.Н., Новокшенов А.А., Соколова Н.В. Острые кишечные инфекции у детей (диагностика, классификация, лечение) // Пособие для врачей. — М. — 2003. — 34с.
3. Мартынова Г.П. Клинико-иммунологические нарушения при кишечных инфекциях у детей и методы их коррекции: Дисс. … д-ра мед.наук. – Красноярск, 2003. — 425 с.
4. Пшенисова А.С., Дарджавия Р.А. Характеристика иммунного статуса при эшерихиозной инфекции у детей // Материалы Второго конгресса педиатров-инфекционистов России «Актуальные вопросы инфекционной патологии у детей. М., 2003. — С. 161-162.
5. Чащина С.Е., Карпова Н.В., Калугина Т.В., Малявина Т.Е., Ахметова Л.И. Микрофлора кишечника и иммунологические показатели в крови у детей, перенесших острый инфекционный энтероколит.// Журнал микр., эпид. и иммунологии. -1997. — №1. — С.87-88.
6. Тихомирова О.В. и др. Вирусные диареи у детей: особенности клинического течения и тактика терапии // Детские инфекции. — 2003. — №3. — С.7-10.
7. Куприна Н.П. и др. Ротавирусная инфекция у детей раннего возраста/ Материалы Второго конгресса педиатров-инфекционистов России «Актуальные вопросы инфекционной патологии у детей. — М., 2003. –С. 101
8. Григорович М.С. Клинико-иммунологическая характеристика ротавирусной инфекции у детей: Дисс. …канд. мед. наук. -М.,1998.-148с.
9. Шендеров Б.А. Медицинская микробная экология и функциональное питание. // Т.1.-Микрофлора человека и животных и ее функции. -М.:ГРАНТЬ, 1998. -288с.
10. Галегов Г.А. // Consillium medicum. – 2002. – Т. 4. – №5. – С. 240–244.
11. Малиновская В.В. Новый комплексный препарат Виферон и его применение в иммунореабилитации в педиатрической и акушерской практике. // International Journal on Immunorehabilitation. — 1998. — №10. — С.76-84.
12. Малиновская В.В., Неумоина М.В., Брагина Г.С. Препараты рекомбинантного альфа-2 интерферона в лечении больных ОВГВ легкого течения // Вопросы вирусологии. — 1997. –Т. 42. — №4. — С.182-185.
13. Чеботарева Т.А. Интерферованный статус и эффективнсть виферона у детей при гриппе и других ОРВИ: Дис. … канд. мед. наук. — М., 2000. -123с.
14. Майкова И.Д. Особенности иммунного статуса и иммунокорригирующая терапия при острых кишечных инфекциях у детей: Дисс. …канд.мед.наук. -М,2007. —
15. Бехтерева М.К., Тихомирова О.В., Железникова Г.Ф. Иммуномодулирующая терапия у детей с иерсиниозной инфекцией // Детские инфекции.-2003. -№2 — С.40-43.
16. Виферон: Руководство для врачей / В.В. Малиновская, Н.В.Деленян, Р.Ю. Ариненко и др. – М.: РАМН ГУ НИИЭМ им. Н.Ф. Гамалеи, 2006. -87с.
17. Blum S, Schiffrin EJ. Intestinal microflora and homeostasis of the mucosal immunt response: Implications for probiotic bateria? In: Probiotics and prebiotics: where are we going? GW Tannock (ed.). Caister Academic press 2002; 10: 311-29.
18. Shindo M. Arai K., Okuno T. Long-term follow-up of hepatitis G virus/GB virus C replication in liver after during and after interferon therapy in patient coinfected with hepatitis C and G viruses. // J. Gastroenterol. — 1999 Dec. — 34 (6). — P.680-687.




