Э.Н. Симованьян, Л.П. Сизякина, А.М. Сарычев, В.Б. Денисенко
Ростовский государственный медицинский университет, Ростов-на-Дону

Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80-100% взрослых. В настоящее время во всем мире отмечается увеличение количества больных ЭБВИ, что связано не только с улучшением качества диагностики, но и с истинным ростом их числа. Заболеваемость острой формой ЭБВИ в различных странах колеблется от 4 до 45 на 100 тыс. населения. Широкому эпидемическому распространению ЭБВИ способствуют большое количество больных и вирусоносителей, а также многообразие путей передачи вируса, к которым относятся воздушно-капельный, контактно-бытовой, половой, парентеральный пути.
ВЭБ является герпесвирусом 4 типа и обладает рядом уникальных биологических свойств. Основными клетками-мишенями для ВЭБ являются В-лимфоциты, с CD21-рецепторами которых связывается этот вирус. Инфицированные В-клетки приобретают способность к неограниченной пролиферации (иммортализация, «клеточное бессмертие») и синтезируют большое количество гетерофильных антител (поликлональная активация). При ЭБВИ возникают изменения не только со стороны В-клеточного звена иммунной системы, но и нарушения клеточного иммунного ответа и факторов врожденной резистентности (макрофагов, NK-клеток, нейтрофилов, системы интерферона). Результатом индукции иммунодефицитного состояния (ИДС) и способности ВЭБ интегрироваться в геном инфицированных клеток является пожизненная персистенция этого вируса.
В настоящее время доказана роль ВЭБ в развитии ряда злокачественных опухолей (лимфомы Беркитта и назофарингеальной карциномы), аутоиммунных заболеваний, синдрома хронической усталости и патологии нервной системы (энцефалитов, менингитов, миелитов, полирадикулонейропатии). Установлена возможность вертикальной трансмиссии возбудителя с развитием врожденной ЭБВИ.

В последние годы пристальное внимание медиков привлекает хроническая форма ЭБВИ, которая развивается у 20% лиц после острой фазы инфекционного процесса. Исследованиями В.А. Зуева (1988) доказано, что продолжительное пребывание вируса в организме человека (персистенция) может протекать в форме латентной, хронической и медленной инфекции (табл. 1).
Латентная инфекция ? бессимптомная персистенция вируса, при которой могут происходить репродукция зрелого вируса и выделение его во внешнюю среду.
Хроническая инфекция ? персистенция вируса, сопровождающаяся появлением одного или нескольких симптомов заболевания с последующим развитием и поддержанием патологического процесса в течение длительного времени.
Медленная инфекция ? персистенция вируса, характеризующаяся его своеобразным взаимодействием с организмом хозяина, при котором, несмотря на развитие патологического процесса, как правило, в одном органе или в одной тканевой системе, имеет место многомесячный и многолетний инкубационный период, после которого медленно, но неуклонно развиваются симптомы заболевания, всегда заканчивающегося летальным исходом.
Таблица 1.
Классификация форм взаимодействия вируса и макроорганизма (В.А. Зуев, 1988)
| Течение инфекционного процесса |
Время пребывания вируса в организме |
|
|
Непродолжительное |
Продолжительное (персистенция) |
|
|
Бессимптомное |
Инаппарантная |
Латентная |
|
С клиническими |
Острая инфекция |
Хроническая инфекция |
Исходами острой ЭБВИ, по данным И.К. Малашенкова и соавт. (2003), являются выздоровление, латентная инфекция и хроническая рецидивирующая ЭБВИ. Исследованиями отечественных и зарубежных авторов установлено, что клиника хронической ЭБВИ у взрослых характеризуется наличием длительных симптомов интоксикации, лимфаденопатии, гепатоспленомегалии, тонзиллита, аденоидита, у части больных ? интерстициальной пневмонии, увеита, гепатита, патологии ЦНС и др. (Ю.В. Лобзин и соавт., 1996; В.В. Краснов, 2003; И.К. Малашенков и соавт., 2003; S.E. Strauss, 1988; P. Kragsbjerg, 1997; S. Yamashita, 1998; S Kuvahara, 2000). Что касается детей, то имеются лишь отдельные работы, посвященные описанию немногочисленных групп больных с хронической ЭБВИ. Кроме того, несмотря на многообразие методов лабораторной диагностики ЭБВИ (серологические методы, молекулярная гибридизация, полимеразная цепная реакция), до настоящего времени нет единства во взглядах ученых на информативность применяемых методик для определения формы и стадии инфекционного процесса.
Следует отметить, что функциональное состояние иммунокомпетентных клеток, их способность к формированию полноценной межклеточной кооперации определяют возможность формирования полноценного иммунного ответа против ВЭБ (Д.В. Стефани, Ю.Е. Вельтищев, 1996; А.В. Караулов, 1999). Персистенция ВЭБ приводит к возникновению ИДС, которое является тем патогенетическим фоном, который формирует контингент «часто и длительно болеющих детей» (В.К. Таточенко, 1995; Н.А. Дидковский, 2002; А.В. Караулов, 2004). Изучение особенностей иммунопатогенеза хронической ЭБВИ у детей позволяет вскрыть тонкие механизмы формирования иммунологической недостаточности, разработать методы диагностики стадий заболевания и дифференцированные схемы терапии данного заболевания.

Таким образом, изучение клинических проявлений, особенностей иммунопатогенеза и выбор оптимального метода диагностики хронической ЭБВИ позволяет сделать еще один шаг к расшифровке причин, формирующих хронические рецидивирующие заболевания у детей, и выработать дифференцированный подход к тактике ведения этих больных.
Нами проведено комплексное клинико-иммунологическое обследование 80 детей в возрасте от 3 до 12 лет жизни с хронической ЭБВИ. Комплексное обследование помимо клинического осмотра больных в динамике включало использование серологических, молекулярно-генетических, бактериологических и иммунологических методов.
С учетом данных серологического обследования методом ИФА (тест-системы «Вектор-Бест», Россия) были выделены следующие подгруппы больных ? реактивация хронической ЭБВИ (VCA-IgM ? пол., EA-IgG ? пол., EBNA-IgG ? пол.), неполная ремиссия (VCA-IgM ? отр., EA-IgG ? отр., EBNA-IgG ? пол.) и атипичная реактивация (VCA-IgM ? пол., EA-IgG ? отр., EBNA-IgG ? пол.). Распределение пациентов с учетом возраста и стадии хронической ЭБВИ представлено на рис. 1.
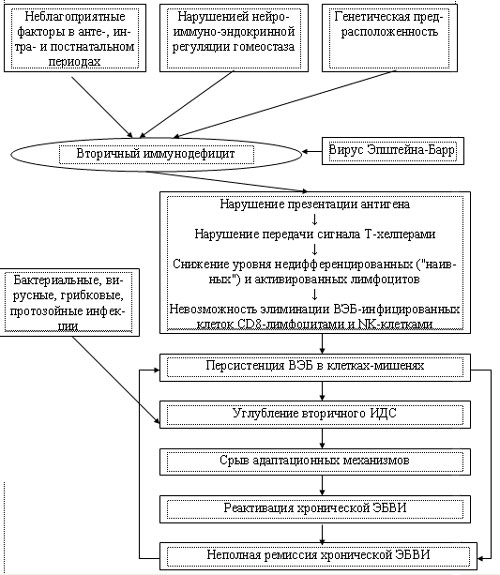
Рис. 1. Распределение больных хронической ЭБВИ с учетом возраста и стадии заболевания.
При обследовании крови методом полимеразной цепной реакции (ПЦР) положительный результат был получен у 12% детей в стадии реактивации, у 22% пациентов в стадии атипичной реактивации и у всех пациентов в стадии неполной ремиссии.
Иммунологическое обследование включало определение CD3-, CD4-, CD8-, HLADR-, CD20-, CD45RA-, CD16- и CD56-лимфоцитов в реакции непрямой иммунофлуоресценции на проточном цитофлуориметре «Epix-XL Coulter» (Франция) с использованием мышиных моноклональных антител (АО «Сорбент ЛТД», Россия). Исследовали сывороточное содержание IgA, IgM, IgG по Манчини с помощью моноспецифических сывороток («ИмБио», Россия). Содержание циркулирующих иммунных комплексов (ЦИК) изучали по В.Ю. Климову (1986). Интенсивность кислород-зависимого метаболизма нейтрофилов оценивали в спонтанном и стимулированном НСТ-тесте (В.В. Менщиков, 1987).
Анализ данных анамнеза жизни обследованных больных выявил отягощенный преморбидный фон у 90% детей (табл. 2). Наиболее часто регистрировались группы риска у матерей пациентов (соматические и инфекционно-воспалительные заболевания в период беременности, патология беременности, осложнения родов и родоразрешения) и у самих больных (последствия перинатального поражения ЦНС, малая мозговая дисфункция, аномалии конституции).
Таблица 2.
Характеристика преморбидного фона больных хронической ЭБВИ (%)
| № |
Фоновая патология |
Дети 3-6 лет |
Дети 7-12 лет |
|
I |
Группы риска у матери |
80 |
94 |
|
1 |
Соматические заболевания |
70 |
25 |
|
2 |
Инфекционные заболевания |
60 |
57,5 |
|
3 |
Отягощенный акушерский анамнез |
80 |
80 |
|
II |
Группы риска у ребенка в постнатальном периоде |
75 |
90 |
|
1 |
Перинатальное поражение ЦНС |
67,5 |
75 |
|
2 |
Постнатальная патология ЦНС (ММД, ВСД) |
― |
20 |
|
3 |
Экссудативный диатез |
17,5 |
17,5 |
|
4 |
Лимфатическая аномалия конституции |
12,5 |
15 |
Все больные относились к группе «часто и длительно болеющих детей» ? количество эпизодов инфекционных заболеваний в течение года колебалось от 6 до 11 (7,9± 1,6). «Пусковыми факторами», приводившими к развитию иммунной дисфункции, являлись перенесенные респираторные инфекции (у 41% пациентов), лакунарная ангина (у 16,3%), острый аденоидит (у 12,5%), лимфаденит (у 10%), документально подтвержденный острый мононуклеоз (у 6,5% детей). Таким образом, персистенции ВЭБ, вероятно, предшествовала субклиническая или легкая форма острого инфекционного процесса.
Результаты обследования больных хронической ЭБВИ показали, что клиническая картина заболевания складывается из интоксикационного, инфекционно-воспалительного, лимфопролиферативного, кардиального и артралгического синдромов (табл. 3).
Таблица 3.
Частота клинических синдромов у детей с хронической ЭБВИ (%)
| Клинические синдромы |
Дети 3-6 лет |
Дети 7-12 лет |
|||
|
Стадия реактива-ции |
Стадия непол-ной ремиссии |
Стадия реактива-ции |
Стадия непол-ной ремиссии |
Стадия атипич-ной реактива-ции |
|
|
1. Инфекционный синдром |
100 |
100 |
100 |
100 |
100 |
|
2. Лимфопролиферативный синдром |
100 |
100 |
100 |
100 |
100 |
|
— Хронический тонзиллит |
100 |
100 |
100 |
100 |
100 |
|
— Хронический аденоидит |
100 |
100 |
100 |
100 |
100 |
|
— Генерализованная лимфаденопатия |
100 |
100 |
100 |
100 |
100 |
|
3. Интоксикационный синдром |
81,2 |
24,2 |
79,3 |
35,7 |
77,8 |
|
4. Астено-вегетативный синдром |
93,7 |
66,7 |
85,7 |
57,8 |
70 |
|
5. Кардиальный синдром |
56,3 |
66,7 |
71,4 |
52,9 |
62,5 |
|
6. Артралгический синдром |
6,3 |
29,2 |
42,9 |
58,8 |
52,5 |
Клиника хронической ЭБВИ у всех пациентов включала лимфопролиферативный синдром (хронический тонзиллит, аденоидит, генерализованная лимфаденопатия), которые сочетались с интоксикационным (у 46,3%), инфекционно-воспалительным (68,8%), астено-вегетативным (75%), кардиальным (62,5%) и артралгическим синдромами (36,3%). Клиническая картина стадии реактивации характеризовалась более высокой частотой интоксикационного (90%) и инфекционно-воспалительного синдромов (88%), стадия атипичной реактивации ? инфекционно-воспалительного (56%), кардиального (63%) и артралгического синдромов (53%), стадия неполной ремиссии ? умеренной выраженностью клинической симптоматики.
Зависимость клинических показателей от возраста детей заключалась в более высокой частоте общеинфекционной симптоматики, воспалительной реакции лимфоидной ткани рото- и носоглотки у детей в возрасте от 3 до 6 лет жизни, в частой регистрации кардиального и артралгического синдромов в старшей возрастной группе.
Бактериологическое исследование микробного пейзажа слизистой ротоглотки у детей с хронической ЭБВИ выявило высокую частоту обнаружения диагностических количеств условно-патогенной микрофлоры (Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus pyogenes, Streptococcus viridans) и грибы рода Candida (табл. 4)
Таблица 4
Характеристика микробного пейзажа слизистой ротоглотки при хронической ЭБВИ у детей (%)
| Микробная флора |
Стадия реактивации |
Стадия неполной ремиссии |
Стадия атипичной реактивации |
Здоровые дети |
|
Streptococcus pyogenes |
57,1 |
41,2 |
55,6 |
10 |
|
Streptococcus viridans |
28,6 |
29,4 |
33,3 |
20 |
|
Staphylococcus aureus |
57,1 |
52,9 |
55,6 |
20 |
|
Staphylococcus epidermidis |
37,5 |
23,5 |
22,2 |
20 |
|
Neisseria spp. |
28,6 |
23,5 |
22,2 |
20 |
|
Candida albicans |
14,3 |
11,8 |
22,2 |
― |
Известно, что характер течения инфекционного процесса определяется особенностями взаимодействия возбудителя и макроорганизма. Причем, ведущую роль в саногенезе играет состояние иммунной системы. В связи с этим представляют интерес данные, полученные при иммунологическом обследовании больных хронической ЭБВИ (табл. 5 и 6).
Таблица 5
Показатели иммунного статуса больных хронической ЭБВИ в возрасте от 3 до 6 лет жизни
| Показатели | Больные хронической ЭБВИ | Здоровые дети | |
|
Стадия реактивации |
Стадия неполной ремиссии |
||
|
CD3,% |
61,2±8,1 |
58,3±9,3 |
60,1±3,4 |
|
CD4,% |
34±3,30 |
32,6±5,30 |
45,2±2,6 |
|
CD8,% |
24,7±2,20,1 |
21,5±4,40 |
16,3±2,7 |
|
CD4/CD8 |
1,3±0,20,1 |
1,5±0,20 |
2,4±0,2 |
|
HLADR,% |
18,5±3,30 |
17,3±4,80 |
9,4±3,2 |
|
CD95,% |
1,2±0,20 |
1±0,10 |
3,2±0,4 |
|
CD16,% |
18,9±2,80,1 |
12,6±4 |
15,1±1,9 |
|
CD56,% |
20,5±6,3 |
21,5±5,6 |
22,5±3,4 |
|
CD45RA,% |
63±5,10 |
57,2±5,20 |
71,4±2,5 |
|
CD20,% |
13,4±7,2 |
13,9±6,8 |
19,3±4,5 |
|
IgA, г/л |
1,2±0,1 |
0,9±0,4 |
1±0,4 |
|
IgM, г/л |
1±0,2 |
0,9±0,3 |
1,1±0,1 |
|
IgG, г/л |
9,4±2,5 |
8,9±2,1 |
10,2±1,5 |
|
ЦИК, усл. ед. |
87,9±22,70 |
85,9±19,50 |
54,5±10,3 |
|
НСТ сп. |
113,1±36,4 |
107,3±32,6 |
99,1±17,7 |
|
К ст. НСТ |
1,5±0,20 |
1,5±0,20 |
1,9±0,1 |
0 – достоверность различий показателей по сравнению со здоровыми детьми
1 – достоверность различий показателей по сравнению со стадией неполной ремиссии
Таблица 6
Показатели иммунного статуса больных хронической ЭБВИ в возрасте от 7 до 12 лет жизни
| Показатели | Больные хронической ЭБВИ | Здоровые дети | ||
| Стадия реактивации |
Стадия неполной ремиссии |
Стадия атипичной реактивации |
||
|
CD3,% |
51,5±4,91,2 |
59,5±4,52 |
72,6±3,60 |
57,3±4,5 |
|
CD4,% |
29,4±5,60,1,2 |
35,4±6,70,2 |
43,8±8,50 |
45,7±4,3 |
|
CD8,% |
24,2±2,10,1 |
21,7±2,90 |
22±3,70 |
16,2±3,3 |
|
CD4/CD8 |
1,2±0,20,1,2 |
1,6±0,40,2 |
2,1±0,60 |
2,5±0,2 |
|
HLADR,% |
22,9±4,60,2 |
16,3±3,4 |
14,3±4,8 |
12,4±3,2 |
|
CD95,% |
0,7±0,070 |
0,1±0,010 |
1,1±0,10 |
4,3±0,3 |
|
CD16,% |
18,9±30,1,2 |
14,6±4 |
10±3,2 |
12,7±1,3 |
|
CD56,% |
25,5±2 |
23,8±4,2 |
26,6±3,1 |
27,4±3,2 |
|
CD45RA,% |
50,4±6,20,2 |
53,8±7,42 |
64±6,60 |
61,4±3,5 |
|
CD20,% |
11,2±5,2 |
12±4 |
10,5±4,2 |
18,3±4,5 |
|
IgA, г/л |
1,4±0,4 |
1,1±0,7 |
1,5±0,5 |
1,1±0,2 |
|
IgM, г/л |
1,2±0,2 |
0,9±0,3 |
1,1±0,2 |
0,9±0,1 |
|
IgG, г/л |
11,8±1,4 |
9,4±1,2 |
10,2±2 |
10,1±1,7 |
|
ЦИК, усл. ед. |
116,5±32,60 |
94,2±32,60 |
76,5±19,2 |
65,2±7,5 |
|
НСТ сп. |
113±36,3 |
114,2±26,6 |
107,8±23,9 |
105,1±27,7 |
|
К ст. НСТ |
1,4±0,20 |
1,5±0,10 |
1,4±0,30 |
2±0,1 |
0 – достоверность различий показателей по сравнению со здоровыми детьми
1 – достоверность различий показателей по сравнению со стадией неполной ремиссии
2 – достоверность различий показателей по сравнению со стадией атипичной реактивации
В стадии реактивации у всех детей независимо от возраста на фоне нормального содержания Т-лимфоцитов (CD3) обнаружено перераспределение их субпопуляционного состава за счет уменьшения числа Т-хелперов (CD4) и увеличения цитотоксических Т-лимфоцитов (CD8), что приводило к уменьшению иммунорегуляторного индекса CD4/CD8 (ИРИ).
Указанные изменения иммунологических показателей характерны для вторичной иммунологической недостаточности по клеточному типу (Д.В. Стефани, Ю.Е. Вельтищев, 1996; А.В. Караулов, 1999; А. Ройт, 2000). У пациентов обеих возрастных групп выявлено увеличение содержания NK-клеток с маркерами CD16 при отсутствии изменений со стороны количества CD56-лимфоцитов. Эти изменения отражали дефект процессов регуляции иммунной системы (Б.В. Пинегин, 1997; А.В. Караулов, 1999; Р.Т. Сепиашвили, 1999; А. Ройт, 2000). У всех пациентов независимо от возраста выявлены изменения функциональной активности иммунокомпетентных клеток, заключающиеся в снижении непримированных (“наивных”) лимфоцитов (CD45RA).
С другой стороны, отмечалось повышение числа HLADR, что свидетельствовало о нарушении процессов поздней активации иммунокомпетентных клеток. Кроме того, у больных младшей и старшей возрастных групп имело место уменьшение готовности лимфоцитов к апоптозу, что документировано снижением количества CD95-клеток. Содержание В-лимфоцитов (CD20), иммуноглобулинов классов IgA, IgM и IgG у всех детей независимо от возраста оставалось в пределах нормы. Регистрировалось повышение содержания ЦИК и снижение адаптационных возможностей кислород-зависимого метаболизма нейтрофилов.
В стадии неполной ремиссии у больных обеих возрастных групп выявлено нормальное количество Т-лимфоцитов, уменьшение ИРИ за счет уменьшения Т-хелперов и увеличения CD8-лимфоцитов. Количество лимфоцитов, экспрессирующих маркеры NK-клеток (CD16 и CD56), оставалось в пределах возрастной нормы. Особенностями иммунного статуса пациентов младшей возрастной группы являлось снижение показателей активации иммунокомпетентных клеток (CD45RA и HLADR), в то время как у больных в возрасте от 7 до 12 лет жизни они были сопоставимыми со здоровыми детьми. У больных младшей и старшей возрастных групп имело место уменьшение готовности лимфоцитов к апоптозу, что документировано снижением количества CD95-клеток. Содержание В-лимфоцитов, IgA, IgM и IgG у всех детей практически не отличалось от возрастной нормы. У всех пациентов отмечалось повышение содержания ЦИК и снижение резервных возможностей кислород-зависимого метаболизма нейтрофилов.
У пациентов в возрасте от 7 до 12 лет жизни с хронической ЭБВИ в стадии атипичной реактивации регистрировалось повышение количества Т-лимфоцитов и CD8-лимфоцитов, нормальное содержание Т-хелперов и уменьшение ИРИ. Содержание NK-клеток, HLADR- и CD45RA-лимфоцитов было сопоставимым с возрастной нормой. Вместе с тем, готовность к апоптозу была сниженной, о чем свидетельствовало уменьшение числа CD95-клеток. Показатели В-клеточного звена иммунной системы (содержание CD20-лимфоцитов, IgA, IgM, IgG, ЦИК) соответствовали нормативным показателям. Регистрировалось снижение резервных возможностей кислород-зависимого метаболизма нейтрофилов.
Анализ показателей иммунного статуса больных хронической ЭБВИ свидетельствует о том, что у данной категории пациентов имеет место вторичное ИДС, которое характеризуется дефектами процессов активации, дифференцировки, снижением ИРИ и готовности к апоптозу иммунокомпетентных клеток, увеличением количества лимфоцитов, обладающих цитотоксическим эффектом. Характер и степень выраженности иммунологических нарушений зависели от стадии заболевания и возраста пациентов. Так, в стадии реактивации имел место дефект всех этапов иммунного ответа. В стадии атипичной реактивации наблюдалось снижение ИРИ и готовности иммунокомпетентных клеток к апоптозу, увеличение количества цитотоксических Т-лимфоцитов. Особенностью иммунного статуса пациентов в стадии неполной ремиссии являлось нарушение процессов активации, снижение ИРИ и готовности клеток к апоптозу, увеличение цитотоксических Т-клеток.
Результаты проведенного нами исследования и сведения современной литературы позволяют представить иммунопатогенез хронической ЭБВИ следующим образом (рис. 2). Неблагоприятные влияние в анте-, интра- и постнатальном периодах развития ребенка приводят к патологии нейро-иммуно-эндокринной регуляции гомеостаза. Встреча иммунокомпрометированного хозяина с ВЭБ не приводит к элиминации последнего ? формируется хроническая (персистирующая) вирусная инфекция. Возникает порочный круг. С одной стороны, стойкий иммунологический дисбаланс способствует длительной персистенции вируса, с другой ? персистенция ВЭБ приводит в нарастанию компенсаторных реакций, истощению адаптационных механизмов и, наконец, к их срывы и усугублению иммунных расстройств. Сформировавшееся вторичное ИДС является тем фоном, на котором развивается цепь последующих инфекционно-воспалительных и паразитарных заболеваний (О.Г. Анджапаридзе, 1984; В.А. Зуев, 1988; А.Н. Маянский, 1998; В.И. Вотяков, 1999; В.В. Абрамов, 2001; S. Strauss, 1992; K. Sugita, 1998).
Формирование хронической ЭБВИ начинается, вероятно, со стадии презентации вирусного антигена макрофагами. Низкий уровень Т-хелперов на фоне дефекта фагоцитарного звена не приводит к полному включению всего комплекса защитных, в первую очередь, клеточных реакций, направленных на элиминацию антигена (D. Moss, 1992; A. Maeda, 1999).
У всех больных хронической ЭБВИ регистрируется повышение количества цитотоксических Т-лимфоцитов. Кроме того, в стадии реактивации повышен уровень NK-клеток. Известно, что при хронической ЭБВИ CD8- и CD16-лимфоциты уничтожают клетки, содержащие вирус в литической фазе (R. Murray, 1992; M. Mizuki, 1998). Однако, длительное увеличение числа этих клеток приводит к разбалансировке иммунной системы и нарастанию клеточной анергии (R. Khanna, 1992). Хронизация процесса свидетельствует о неэффективности клеточной и антителозависимой цитотоксичности, интерферонодефиците (J. Anderson, 1996; F. Schwarzman, 1998). С другой стороны, снижение количества «наивных» CD45RA-лимфоцитов и повышение клеток, несущих маркер поздней активации (HLADR) свидетельствуют о сохраняющейся полноценности процессов активации иммунокомпетентных клеток (S. Ohga, 1999).
Известно, что элиминация ВЭБ-инфицированных клеток осуществляется с участием процесса апоптоза. Низкий уровень презентации CD95-рецептора на клеточной мембране лимфоцитов, обнаруженный у всех пациентов независимо от возраста и стадии заболевания, свидетельствует об угнетении CD95-зависимого апоптоза и способствует сохранению популяции ВЭБ-инфицированных клеток (Г.Ф. Железникова, 2000; S. Kirchhoff, 2000).
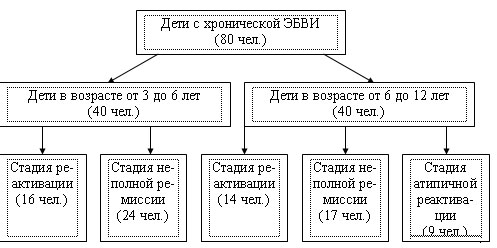
Рис. 2. Иммунопатогенез хронической ЭБВИ у детей.
Нарушения иммунного статуса являются тем патогенетическим фоном, который приводит к длительной персистенции ВЭБ в клетках-мишенях. Возникший вторичный иммунодефицит способствует активации условно-патогенной микрофлоры, вирусных и грибковых заболеваний. Так, при анализе микробного пейзажа слизистой ротоглотки у больных хронической ЭБВИ достаточно часто выявлялась условно-патогенная микрофлора (Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus pyogenes, Streptococcus viridans) и грибы рода Candida. Данное обстоятельство, по мнению ряда авторов, также может служить косвенным признаком ИДС (В.В. Ботвиньева, 199; Т.И. Долгих, 1999; А.В. Караулов, 2004).
Анализ результатов клинико-иммунологических сопоставлений, серологического и молекулярно-генетического исследования, обобщение данных современной литературы позволяют выделить три варианта течения хронической ЭБВИ (рис.3).
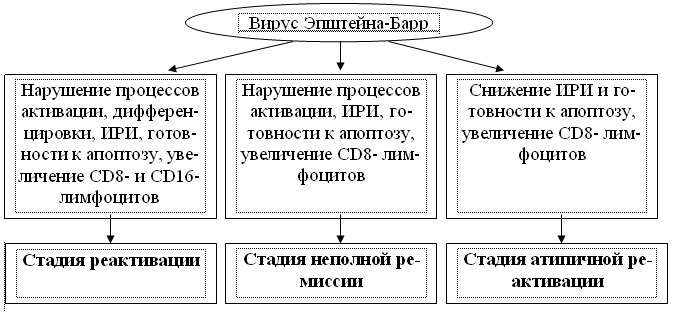
Рис. 3. Варианты хронической ЭБВИ у детей.
Стадия реактивации хронической ЭБВИ у всех пациентов характеризуется положительным результатом ИФА (VCA-IgM +, EA-IgG +, EBNA-IgG +), у 12% ? положительным результатом ПЦР крови. Клиническая симптоматика включает интоксикационный, астено-вегетативный и лимфопролиферативный синдромы, максимально выраженные у больных с положительной ПЦР. Иммунная дисфункция выражается в нарушении процессов активации и дифференцировки, снижении ИРИ и готовности клеток к апоптозу, увеличении CD8- и CD16-лимфоцитов.
Лабораторными маркерами стадии неполной ремиссии у всех пациентов являются обнаружение высоких титров EBNA-IgG при отсутствии VCA-IgM и EA-IgG, а также выявление ДНК вируса в крови. Спектр клинических синдромов соответствует стадии реактивации, однако они выражены в меньшей степени. Иммунная дисфункция проявляется преимущественным нарушением активации, снижением ИРИ, готовности к апоптозу и увеличением количества CD8- лимфоцитов.
Показателями стадии атипичной реактивации у всех пациентов являются обнаружение VCA-IgM и EBNA-IgG при отсутствии EA-IgG, у 22% ? положительная ПЦР крови. Характер основных клинических синдромов у этих детей в целом соответствует таковым в стадии реактивации. Максимальная степень выраженности симптоматика достигает у детей с положительной ПЦР. Иммунные сдвиги характеризуются снижением ИРИ, готовности к апоптозу и увеличением CD8- лимфоцитов.
На основании результатов проведенного исследования разработан алгоритм диагностики хронической ЭБВИ у детей (рис. 4).
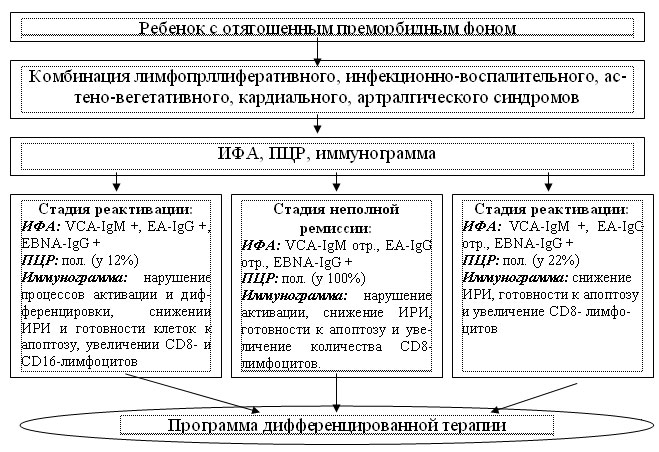
Рис. 4. Алгоритм диагностики хронической ЭБВИ у детей.
Принципы лечения хронической ЭБВИ
Базисная терапия
1.Охранительный режим
2. Лечебное питание
3. Противовирусные препараты:
- Вироцидные препараты ? изопринозин, аномальные нуклеозиды (валтрекс, фамвир, ацикловир), арбидол (табл. 7)
- Препараты интерферона ? виферон, кипферон, реаферон-ЕС-липинт, интерфероны для в/м введения (реаферон, реальдирон, интрон А, роферон А) (табл. 8 и 9)
- Индукторы интерферона ? амиксин, циклоферон, неовир, анаферон (табл. 10)
4. Локальные антибактериальные препараты ? биопарокс, ИРС-19, рибомунил, имудон, лизобакт, гексорал, стопангин и др.
5. Витаминно-минеральные комплексы ? сана-сол, мульти-табс, витрум, центрум, киндер-биовиталь и др.
Таблица 7.
Вироцидные препараты, применяемые для лечения хронической ЭБВИ
| Наименование |
Легкая и среднетяжелая форма |
Тяжелая форма |
Возраст |
|
Изопринозин |
50-100 мг/кг/сут в 4 приема внутрь 7-10 дней |
100 мг/кг/сут в 4 приема внутрь, 3 курса по 10 дней с интервалом 10 дней |
С первых дней жизни |
|
Арбидол |
У детей от 2 до 6 лет по 50 мг, от 6 до 12 лет ― по 100 мг, старше 12 лет ― по 200 мг 4 раза в день внутрь в течение 7 дней, затем 2 раза в неделю в течение 4 недель. |
С 2 лет |
|
|
Валтрекс |
10 мг/кг/сут в 2 приема внутрь 5-10 дней |
10 мг/кг/сут в 2 приема внутрь 10 дней |
С 2 лет |
|
Фамвир |
По 500 мг 3 раза в день внутрь 5-7 дней |
По 500 мг 3 раза в день внутрь 7-10 дней |
С 12 лет |
|
Ацикловир (при отсутствии других препаратов) |
До 2 лет по 200 мг 5 раз в день, старше 2 лет ― по 400 мг 5 раз в день внутрь 5-10 дней |
До 2 лет по 200 мг 5 раз в день, старше 2 лет ― по 400 мг 5 раз в день внутрь, или 10 мг/кг в/в кап. 3 раза в день 7-10 дней |
С первых дней жизни |
Таблица 8.
Схемы стартовой терапии хронической ЭБВИ препаратами интерферона
| Наименование |
Легкая и среднетяжелая формы |
Тяжелая форма |
Возраст |
|
Виферон |
Детям до 1 года виферон-1, от 1 до 7 лет ― виферон-2, от 7 до 14 лет ― виферон-3, старше 14 лет ― виферон-4 по 1 св. 2 раза в день 5-10 дней с последующим переходом на поддерживающую терапию |
Детям до 1 года виферон-1, от 1 до 7 лет ― виферон-2, от 7 до 14 лет ― виферон-3, старше 14 лет ― виферон-4 по 1 св. 2 раза в день 10 дней с последующим переходом на поддерживающую терапию |
С первых дней жизни |
|
Кипферон |
Детям до 1 года 1/2 св., от 1 до 7 лет ― 1 св., от 7 до 14 лет ― 2 св. 2 раза в день 5-10 дней с последующим переходом на поддерживающую терапию |
Детям до 1 года 1/2 св., от 1 до 7 лет ― 1 св., от 7 до 14 лет ― 2 св. 2 раза в день 10 дней с последующим переходом на поддерживающую терапию |
С первых дней жизни |
|
Реаферон-ЕС-липинт |
― |
Детям 2-3 лет по 250 тыс. ЕД, старше 3 лет ― по 500 тыс. ЕД 2 раза в день внутрь 10-20 дней с последующим переходом на поддерживающую терапию |
Старше 2 лет |
|
Интерфероны для в/м введения |
― |
По 500 тыс.- 2 млн ЕД в/м 1 раз в день 10-14 дней с последующим переходом на поддерживающую |
Старше 2 лет жизни |
Таблица 9.
Схемы поддерживающей терапии хронической ЭБВИ препаратами интерферона1
| Препараты |
Схемы терапии2 |
|
Виферон |
Виферон в возрастной дозе по 1 св. 2 раза в день 3 раза в неделю ― 3-12 месяцев |
|
Интерфероны для в/м введения3 |
По 500 тыс.- 2 млн ЕД в/м 3 раза в неделю ― 3-6 месяцев |
Примечания.
1 ? поддерживающая терапия препаратами интерферона назначается после стартовой терапии.
2 ? продолжительность поддерживающей терапии определяют с учетом клинико-лабораторных показателей активности хронической ЭБВИ.
3 ? интерфероны для в/м введения применяют только у детей старше 2 лет жизни при тяжелой форме хронической ЭБВИ.
Таблица 10.
Индукторы интерферона, применяемые для лечения хронической ЭБВИ
| Препараты |
Доза, пути введения, возраст пациентов |
Схемы лечения |
|
Циклоферон |
По 6-10 мг/кг в/м, внутрь детям старше 4 лет |
Два-три базовых курса с интервалом в 2-3 недели. |
|
Неовир |
По 4-6 мг/кг в/м детям с первых дней жизни |
Однократное введение препарата ежедневно №2, затем через день №3, затем переход на поддерживающие месячные курсы по 1 инъекции в неделю с интервалом в 1 месяц |
|
Амиксин |
По 60 мг/сут внутрь детям старше 7 лет |
Ежедневно №2, затем через день №18 |
|
Анаферон |
По 1 табл. под язык |
В первый день в течение двух часов по 1 табл. каждые 30 мин., затем 3 табл. через равные промежутки времени; со вторых суток ― по 1 табл. 3 раза в день до выздоровления |
Примечания.
Показания к применению индукторов интерферона: а). в качестве стартовой терапии ? при легких и среднетяжелых формах; б). в качестве поддерживающей терапии ? после курса вироцидных препаратов и интерферонов.
Интенсификация лечения хронической ЭБВИ
Иммунотерапия под контролем иммунограммы ? иммуномодуляторы (тималин, тактивин, тимоген, имунофан, полиоксидоний, ликопид, деринат, нуклеинат натрия, нейпоген, ИРС-19, рибомунил, бронхомунал, иммуномакс и др.), цитокины (ронколейкин, лейкинферон).
Пробиотики ? бифиформ, бифидум-бактерин-форте, пробифор, линекс и др.
Препараты метаболической реабилитации ? актовегин, солкосерил, элькар, лимонтар, реамберин и др.
Энтеросорбенты ? смекта, фильтрум, энтеросгель, полифепан и др.
Антигистаминные препараты 2 поколения (кларитин, зиртек, фенистил, эриус, телфаст и др.) ? по показаниям.
Гепатопротекторы (эссенциале, гептрал, урсосан, карсил, хофитол, гепабене, гепатофальк и др.) ? по показаниям.
Нейро- и ангиопротекторы (энцефабол, глиатилин, инстенон, кавинтон, циннаризин и др.) ? по показаниям.
Кардиотропные препараты (рибоксин, кокарбоксилаза, цитохром С и др.) ? по показаниям.
Антигомотоксические и гомеопатические средства ? лимфомиозот, тонзилла композитум и др.
ФТЛ ? массаж, ЛФК, иглорефлексотерапия и др.
Симптоматическая терапия
При затруднении носового дыхания назначают назальные препараты ? изофра, полидекса, називин, виброцил, адрианол и др.
При наличии сухого кашля назначают противокашлевые препараты (глаувент, туссупрекс, либексин, бутамират и др.), при влажном кашле ? отхаркивающие и муколитические препараты (амброгексал, бромгексин, ацетилцистеин, мукалтин, бронхикум и др.).
Нами проведена оценка эффективности комплексного лечения хронической ЭБВИ у детей с использованием вироцидного и иммуномодулирующего препарата изопринозина в сочетании с препаратами интерферона. Проведено клинико-иммунологическое и серологическое обследование 65 детей в возрасте от 6 до 13 лет жизни с хронической ЭБВИ в стадии реактивации. В первую группу вошли 30 детей, получавших виферон по пролонгированной схеме, во вторую ?35 пациентов, которым помимо виферона был назначен изопринозин в дозе 50-100 мг/кг/сут внутрь (3 курса по 10 дней с интервалом 10 дней).
Через три месяца после начала лечения у 70% больных первой группы наблюдалась положительная динамика клинико-лабораторных показателей. У 33,3% детей отмечалось уменьшение размеров лимфоузлов, у 50% ? размеров глоточных миндалин, у 70% пациентов ? размеров небных миндалин. У 70% больных регистрировалось исчезновение VCA-IgM и EA-IgG. Со стороны иммунного статуса имела место тенденция к увеличению CD4- и CD95-лимфоцитов. Вместе с тем, сохранялись увеличение числа CD8- и HLA-DR-лимфоцитов, уменьшение количества CD45RA-клеток, повышение содержания ЦИК и редукция резервных возможностей кислород-зависимого метаболизма нейтрофилов (НСТ-тест).
У пациентов второй группы клинико-лабораторная эффективность комплексного лечения была более высокой ? 85,7%. Через три месяца после начала лечения уменьшение размеров лимфоузлов отмечено у 51,4% детей, уменьшение размеров глоточных миндалин ? у 65,7%, небных миндалин ? у 85,7% пациентов. У 85,6% больных наблюдалось исчезновение VCA-IgM и EA-IgG. Происходило восстановление количества CD4-, CD8-, CD45RA-, HLA-DR- и CD95-лимфоцитов, снижение содержания ЦИК и увеличение адаптационных возможностей кислород-зависимого метаболизма нейтрофилов.
Результаты проведенного исследования свидетельствуют о том, что сочетанное использование изопринозина и виферона в качестве противовирусных препаратов приводит к более существенной положительной динамике со стороны клинических симптомов хронической ЭБВИ, исчезновению серологических маркеров активности инфекционного процесса и восстановлению измененных показателей иммунного статуса.
Диспансерное наблюдение за больными хронической ЭБВИ
Диспансеризация проводится участковым врачом и инфекционистом. Продолжительность диспансерного наблюдения составляет до 6 месяцев после исчезновения клинико-лабораторных показателей активности инфекционного процесса. Кратность осмотров 1 раз в месяц. По показаниям проводят консультацию специалистов (гематолог, ЛОР-врач, иммунолог, онколог и др.). Лабораторно-инструментальное обследование включает
1. Общий анализ крови 1 раз в месяц в течение 3 месяцев, затем 1 раз в 3 месяца, по показаниям ? чаще;
2. Серологические маркеры ЭБВИ1 раз в 3 месяца, по показаниям ? чаще;
3. ПЦР крови, мазков из ротоглотки 1 раз в 3 месяца, по показаниям ? чаще;
4. Иммунограмма ? 1 раз в 3-6 месяцев;
5. Биохимическое исследование(билирубин, АЛТ, АСТ, тимоловая проба, общий белок, белковые фракции, сиаловые кислоты, С-реактивный белок и др.) ? по показаниям;
6. Инструментальное обследование (УЗИ органов брюшной полости, нейросонография, допплерометрия, ЭЭГ, РЭГ, РКТ, МРТ и др.) ? по показаниям.
Таким образом, хроническая ЭБВИ относится к наиболее актуальным проблемам современной педиатрии и детской инфектологии, что связано с широким эпидемических распространением заболевания, длительным течением с периодической реактивацией инфекционного процесса, возможностью развития осложнений и неблагоприятных исходов (онкозаболевания, аутоиммунная патология), трудностями в диагностике, лечении и профилактике. В основе патогенеза хронической ЭБВИ, помимо биологической свойств самого возбудителя, важную роль играет состояние макроорганизма. Отягощенный преморбидный фон в сочетании с иммунотропной активностью ВЭБ способствуют формированию вторичного ИДС, которое характеризуется нарушением процессов активации, дифференцировки, снижением ИРИ и готовности к апоптозу иммунокомпетентных клеток, увеличением количества лимфоцитов, обладающих цитотоксическим потенциалом.
С учетом особенностей преморбидного фона и иммунного статуса формируются три варианта хронической ЭБВИ ? реактивация, атипичная реактивации и неполная ремиссия. К ведущим клиническим синдромам хронической ЭБВИ у детей относятся инфекционно-воспалительный, лимфопролиферативный, интоксикационный, астено-вегетативный, кардиальный и артралгический синдромы. Диагностика хронической ЭБВИ в детском возрасте основана на анализе групп риска, выделении ведущих клинических синдромов и лабораторном обследовании (ИФА, ПЦР, иммунограмма).
Лечение хронической ЭБВИ должно быть комплексным и включать этиотропные средства (вироцидные препараты, интерфероны и их индукторы), препараты патогенетической, иммуномодулирующей, симптоматической и сопроводительной терапии. Причем, сочетанное использование лекарственных средств, воздействующих на различные этапы репликации вируса (изопринозин, виферон), существенно повышает эффективность лечения. Больные хронической ЭБВИ нуждаются в длительном диспансерном наблюдении с обязательным контролем лабораторных маркеров активности инфекционного процесса.




